

分析 Ⅰ.生铁中含有碳杂质,在电解质环境下,铁发生电化学腐蚀,若溶液呈酸性则发生析氢腐蚀,若溶液呈中性则发生吸氧腐蚀,左边试管中是中性溶液,发生吸氧腐蚀,右边试管中是酸性溶液发生析氢腐蚀,据此解答;
Ⅱ.(1)原电池的负极金属易被腐蚀,根据原电池的工作原理来回答;
(2)在电解池的阴极上的金属被保护,根据电解池的工作原理来回答;
(3)电解池的保护比原电池保护更好判断.
解答 解:Ⅰ.生铁中含有碳杂质,在电解质环境下,铁发生电化学腐蚀;故答案为:电化学;
(1)红墨水柱两边的液面变为左低右高,则a发生析氢腐蚀,b发生吸氧腐蚀,所以b边盛有食盐水,故答案为:b;
(2)b试管中铁发生的是吸氧腐蚀,生铁中碳上发生的电极反应式O2+2H2O-4e-=4OH-;负极发生氧化反应,电极反应式为:Fe-2e-=Fe2+,所以b试管中铁被腐蚀的总化学方程式为2Fe+O2+2H2O=2Fe(OH)2;故答案为:吸氧;O2+2H2O-4e-=4OH-;2Fe+O2+2H2O=2Fe(OH)2;
Ⅱ.(1)为了降低某水库的铁闸门被腐蚀的速率,可以让金属铁做原电池的正极,其中焊接在铁闸门上的固体材料R可以是比金属铁的活泼性强的金属,钠不能做电极材料,所以选锌,此方法叫做牺牲阳极的阴极保护法,故答案为:C;牺牲阳极的阴极;
(2)电解池的阴极上的金属被保护,为降低铁闸门的腐蚀速率,其中铁闸门应该连接在直流电源的负极,故答案为:负;
(3)因为电解池的保护比原电池保护更好,所以乙种能使铁闸门保护得更好;
故答案为:乙.
点评 本题考查了金属的腐蚀与防护,明确原电池和电解池原理是解本题关键,知道作原电池负极和电解池阳极的金属易被腐蚀,难度不大.


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:解答题
 .
.
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 混合气体中一定含有甲烷 | B. | 混合气体一定是甲烷和乙烯 | ||
| C. | 混合气体中一定含有乙烷 | D. | 混合气体可能是甲烷和乙烯 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Ba(OH)2•8H2O与NH4C1反应 | B. | 水解反应 | ||
| C. | 醋酸的电离 | D. | 盐酸与NaOH溶液的反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 硬脂酸与软脂酸(C15H31COOH) | B. | HCHO与CH3COOH | ||
| C. | CH2=CHCOOH与CH3CH2CH2COOH | D. | 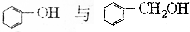 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
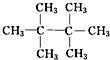
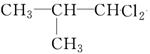 、
、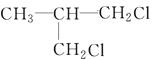 、
、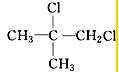 .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
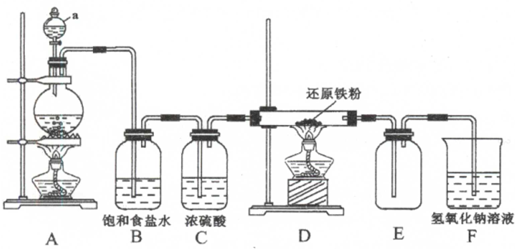
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com