
 ;
; .
.


 夺冠金卷全能练考系列答案
夺冠金卷全能练考系列答案科目:高中化学 来源: 题型:
| A、① | B、①④ | C、①③ | D、②③ |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、日常生活中看到的烟、云、雾 |
| B、明矾可做净水剂 |
| C、向FeCl3溶液中滴加烧碱溶液,得到红褐色浑浊的分散系 |
| D、向沸水中逐滴加入FeCl3饱和溶液,得到红褐色透明的分散系 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、②⑤⑨ | B、①②⑤⑦⑨ |
| C、②⑤⑥⑦⑨ | D、全部正确 |
查看答案和解析>>
科目:高中化学 来源: 题型:
 按图装置实验,若x轴表示流入正极的电子的物质的量,忽略溶液体积的变化;则y轴应表示( )
按图装置实验,若x轴表示流入正极的电子的物质的量,忽略溶液体积的变化;则y轴应表示( )| A、①②③ | B、②③⑤ |
| C、①②④ | D、仅② |
查看答案和解析>>
科目:高中化学 来源: 题型:


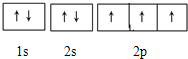

查看答案和解析>>
科目:高中化学 来源: 题型:
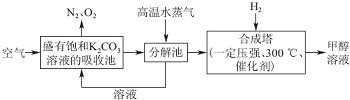
| A、碳酸钾溶液所起的作用是富集空气中的CO2 | ||||
B、分解池中发生反应的化学方程式为:2KHCO3
| ||||
| C、上述流程中能循环利用的物质有碳酸钾溶液和空气 | ||||
| D、合成塔中生成甲醇的反应,其原子利用率理论上可以达到100% |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、55.2 kJ |
| B、391 kJ |
| C、336 kJ |
| D、1.39 kJ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com