
[选修—化学与技术](15分)
水是一种重要的自然资源,是人类赖以生存不可缺少的物质。水质优劣直接影响人体健康。请回答下列问题:
(1)天然水中溶解的气体主要有 、 。
(2)天然水在净化处理过程中加入的混凝剂可以是 其纯净水作用的原理是
(3)水的纯净和软化的区别是
(4)硬度为![]() 的水是指每升水含10
的水是指每升水含10![]() 或与之相当的物质(如7.1
或与之相当的物质(如7.1![]() )。若某天然水中
)。若某天然水中![]() ,
,![]() ,则此水的硬度为 ;
,则此水的硬度为 ;
(5)若(4)中的天然水还含有![]() ,现要软化10
,现要软化10![]() 这种天然水,则需先加入
这种天然水,则需先加入![]()
![]() ,后加入
,后加入![]()
![]() 。
。
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:阅读理解
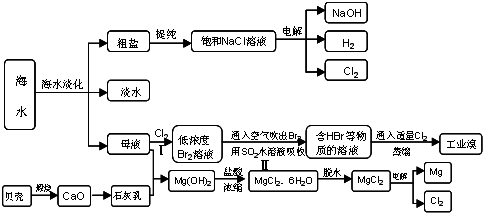
查看答案和解析>>
科目:高中化学 来源: 题型:阅读理解

查看答案和解析>>
科目:高中化学 来源: 题型:阅读理解

 (1)写出设备A、B的名称:A
(1)写出设备A、B的名称:A查看答案和解析>>
科目:高中化学 来源: 题型:
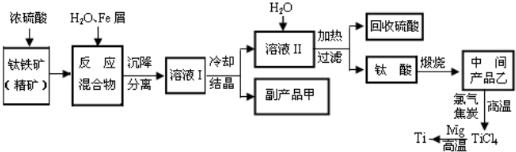
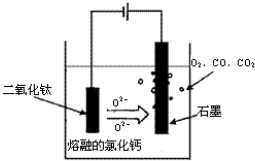
查看答案和解析>>
科目:高中化学 来源: 题型:
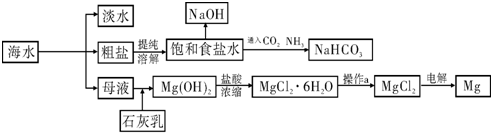
| MgO | MgCl2 | |
| 熔点/℃ | 2852 | 714 |
| 沸点/℃ | 3600 | 1412 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com