
| A、K+:1s22s22p63s23p6 |
| B、F:1s22s22p5 |
| C、S2-:1s22s22p63s23p4 |
| D、Ar:1s22s22p63s23p6 |


科目:高中化学 来源: 题型:
| A、浓硫酸有氧化性,稀硫酸没有氧化性 |
| B、CO2和SO2都是酸性氧化物,与NaOH溶液反应均可生成两种盐 |
| C、常温下浓硝酸和稀硝酸均可用铁质容器盛装 |
| D、澄清石灰水可用来鉴别Na2CO3和NaHCO3溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、多电子原子轨道能量高低:4s>3p>3s>2px=2py |
| B、硬度由大到小:金刚石>碳化硅>晶体硅 |
| C、熔点由高到低:NaCl>SiO2>Hg>P4 |
| D、晶格能由大到小:KF>KCl>KB>KI |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、FeCl3溶液与Cu的反应:Cu+Fe3+═Cu2++Fe2+ |
| B、NO2与水的反应:3NO2+H2O═2NO3-+NO+2H+ |
| C、醋酸溶液与水垢中的CaCO3反应:CaCO3+2H+═Ca2++H2O+CO2↑ |
| D、稀硝酸与锌粒反应:Zn+2H+═Zn+H2↑ |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、只含离子键的化合物形成的晶体才是离子晶体 |
| B、(NH4)2SO4晶体是含有离子键、共价键和配位键的晶体 |
| C、由于I-I共价键键能比F-F、Cl-Cl、Br-Br的都弱,因此在卤素单质中I2的熔点、沸点最低 |
| D、在分子晶体中一定不存在离子键,在离子晶体中也一定不存在共价键 |
查看答案和解析>>
科目:高中化学 来源: 题型:
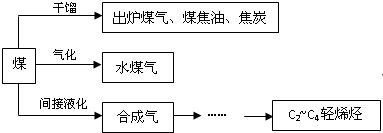
查看答案和解析>>
科目:高中化学 来源: 题型:
 A、B、C均为中学所学的常见物质且均含有同一种元素,X为金属单质,A为气体单质,它们之间的转化关系如图所示(反应条件及其他物质已经略去):
A、B、C均为中学所学的常见物质且均含有同一种元素,X为金属单质,A为气体单质,它们之间的转化关系如图所示(反应条件及其他物质已经略去):查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com