
【题目】某混合物A,含有KAl(SO4)2、Al2O3和Fe2O3,在一定条件下可实现如图所示的物质之间的变化:
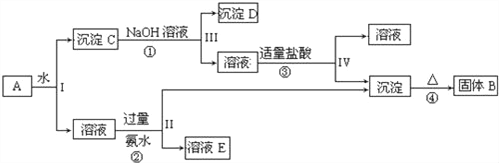
据此回答下列问题:
(1)Ⅰ、Ⅱ、Ⅲ、Ⅳ四步中对于溶液和沉淀的分离采取的方法是_____.
(2)根据上述框图反应关系,写出下列B、C、D、E所含物质的化学式
沉淀固体B______;C________;沉淀D_____;溶液E________.
(3)写出①、②、③、④四个反应方程式
①_________________________;
②________________________;
③________________________;
④________________________.
【答案】过滤Al2O3Al2O3、Fe2O3Fe2O3K2SO4、(NH4)2SO4Al2O3+2NaOH+3H2O=2Na[Al(OH)4]2KAl(SO4)2+6 NH3.H2O=K2SO4+3(NH4)2SO4+2Al(OH)3↓Na[Al(OH)4]+HCl=NaCl+H2O+Al(OH)3↓2Al(OH)3![]() Al2O3+3H2O
Al2O3+3H2O
【解析】
KAl(SO4)2溶于水,Al2O3和Fe2O3均不溶于水,混合物A加水溶解后,溶液中是KAl(SO4)2,沉淀C为Al2O3和Fe2O3;由转化关系图可知,向沉淀C中加NaOH溶液,Fe2O3不反应,沉淀D为Fe2O3,Al2O3可与NaOH溶液反应生成NaAlO2,向NaAlO2溶液中通入CO2可得Al(OH)3沉淀,Al(OH)3受热分解生成固体B为Al2O3;向溶液中加过量氨水,溶液与过量氨水反应,Al3+被沉淀,得到氢氧化铝沉淀,溶液中E为K2SO4、(NH4)2SO4,经过蒸发、结晶,得到K2SO4和(NH4)2SO4;
(1)溶液和沉淀的分离利用过滤;
(2)由上述分析可知B为Al2O3,C为Al2O3、Fe2O3,D为Fe2O3溶液E为K2SO4、(NH4)2SO4;
(3)反应①为Al2O3+2NaOH+3H2O=2Na[Al(OH)4],
反应②为2KAl(SO4)2+6NH3.H2O=K2SO4+3(NH4)2SO4+2Al(OH)3↓,
反应③为Na[Al(OH)4]+HCl=NaCl+H2O+Al(OH)3↓,
反应④为2Al(OH)3![]() Al2O3+3H2O。
Al2O3+3H2O。


 孟建平小学滚动测试系列答案
孟建平小学滚动测试系列答案 黄冈天天练口算题卡系列答案
黄冈天天练口算题卡系列答案科目:高中化学 来源: 题型:
【题目】在一定体积的容器中加入1.5mol氙气(Xe)和7.5mol氟气(F2),于400℃和2633kPa压强下加热数小时,然后迅速冷却至25℃,容器内除得到一种无色晶体外,还余下4.5mol氟气,则所得无色晶体产物中,氙与氟的原子个数之比是
A.1∶2 B.1∶3 C.1∶4 D.1∶6
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】MnO2是一种重要的无机功能材料,粗MnO2的提纯是工业生产的重要环节.某研究性学习小组设计了将粗MnO2(含有较多的MnO和MnCO3)样品转化为纯MnO2实验,其流程如下
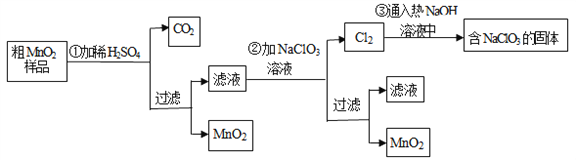
(1)第①步加稀H2SO4时,粗MnO2样品中的_____________(写化学式)转化为可溶性物质.
(2)第②步反应的离子方程式:_______________________
(3)流程中得到MnO2固体操作必需的玻璃仪器有玻璃棒、烧杯、_______________。
(4)已知第③步蒸发得到的固体中有NaClO3和NaOH,则一定还有含有_________(写化学式).其中用到Cl2的实验室制法的反应离子方程式:_______________________。
(5)若粗MnO2样品的质量为50.76g,第①步反应后,经过滤得到34.8gMnO2,并收集到0.896LCO2(标准状况下),则在第②步反应中至少需要____________ gNaClO3.[M (NaClO3)=106.5]
(6)第①步酸溶产生的CO2与NH3反应可合成化肥尿素[化学式为CO(NH2)2]。己知:
①2NH3(g)+CO2(g)=NH2CO2NH4(s); ΔH=-159.5kJ·mol-1
②NH2CO2NH4(s)=CONH2)2(s)+H2O(g); ΔH=+116.5kJ·mol-1
③H2O(l)=H2O(g) ΔH=+44.0kJ·mol-1
写出CO2与NH3合成尿素和液态水的热化学反应方程式______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某无色溶液中可能含有Na+、NH4+、Ba2+ 、Cu2+、SO42-、SO32-、Cl-、Br-、CO32-中的若干种,为检验其中含有的离子,进行如下实验:
①取10 mL溶液,加入足量氯水,无气体产生,再加入CCl4溶液分层,下层为橙红色;
②分液后,将①中上层溶液加入足量BaCl2和HCl溶液,产生白色沉淀2.33g;
③另取10mL原溶液,加入过量的浓氢氧化钠溶液并加热,收集到标准状况下448mL气体。下列关于原溶液的说法正确的是
A. 肯定存在NH4+、Cl-、Br- B. 是否存在Na+需要通过焰色反应来确定
C. SO42-、SO32-至少含有一种 D. 肯定不存在Ba2+、Cu2+、SO32-、CO32-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】为提纯下列物质(括号内为杂质),所用的除杂试剂和分离方法都正确的是( )
序号 | 不纯物 | 除杂试剂 | 分离方法 |
A | CH4(C2H4) | 酸性KMnO4溶液 | 洗气 |
B | 苯(苯酚) | 浓溴水 | 过滤 |
C | C2H5OH(H2O) | 新制生石灰 | 蒸馏 |
D | 乙醇(乙酸) | 饱和Na2CO3溶液 | 分液 |
A. A B. B C. C D. D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现有一瓶1 000 mL、含25% NaClO、密度是1.19 g.cm-3的“84消毒液”,使用时需要稀释100倍(体积比),密封保存。下列分析不正确的是
A. 该“84消毒液”中NaClO物质的量浓度为4.0 mol·L-l
B. 该“84消毒液”稀释100倍后,Na+的物质的量浓度为0. 04 mol·L-l
C. 空气中的CO2与“84消毒液”发生反应的化学方程式是NaClO+CO2+H2O= NaHCO3+ HClO
D. 用容量瓶配制上述浓度的“84消毒液”480 mL,需要称量的NaClO固体质量为143.0 g
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】关于烷烃和烯烃相比较,不正确的是( )
A.能用CnH2n+2通式表示的烃一定是烷烃,而符合CnH2n的烃一定是烯烃
B.烷烃不能与酸性高锰酸钾溶液和溴水反应而褪色,但烯烃可以
C.烷烃属于饱和链烃,烯烃属于不饱和链烃
D.乙烯分子中的碳、氢原子都处在同一平面上,而乙烷分子中的碳、氢原子不都处在同一平面上
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】CuCl广泛应用于化工和印染等行业。某研究性学习小组拟热分解CuCl2·2H2O制备CuCl,并验证其它分解产物。
【查阅资料】
①![]()
②CuCl是一种白色难溶固体,潮湿CuCl在空气中缓慢被氧化
⑴配平潮湿CuCl在空气中被氧化的化学方程式_________
____CuCl+_____O2+_____□=_______3CuO·CuCl2·3H2O+______HCl
【实验探究】该小组选用下图装置进行实验(夹持加热仪器略)。

⑵装置A用于制取HCl:NaCl+H2SO4=NaHSO4+HCl↑,浓硫酸在该反应中体现强酸性和_________性;
⑶按实验要求选择上图装置,连接顺序为:a_______(按气流方向,用小写字母表示);
⑷根据完整的实验装置进行实验,实验步骤如下:
①连接装置,_______;②装入药品;③打开分液漏斗活塞;④控制温度加热硬质玻璃管一段时间;⑤停止通HCl,升温继续加热;…
步骤①是__________________;步骤④通HCl的目的是_________________;
⑸装置E中发生反应的离子方程式是______________________。
【实验分析与改进】
⑹装置B中试纸先变蓝后又褪色,经查资料获知过量的Cl2能将I2氧化。甲同学认为可将湿润的淀粉KI试纸改成足量的淀粉KI溶液以克服Cl2过量的问题,但小组分析后认为该方案存在一个明显安全问题:_____________________
⑺反应结束后,CuCl产品中可能含有少量未分解的CuCl2,乙同学认为只用一种日常生活常见的液体即可检验。该实验方案为:取少量固体放入小试管中,_________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com