
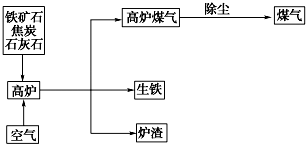
分析 (1)铁矿石、焦炭和石灰石从炉顶装入而空气从高炉下部吹入,使反应物充分接触,提高原料利用率;
(2)现代炼铁在鼓入空气的同时会喷入煤粉,减少焦炭用量,降低成本;
(3)煅烧石灰石生成氧化钙和二氧化碳,氧化钙和二氧化硅反应生成硅酸钙,氧化钙和二氧化硫反应生成亚硫酸钙.
解答 解:(1)高炉炼铁时原料的加入方法是:铁矿、焦炭、石灰石从炉顶投入,而高温的空气从炉底通入,这样原料和空气可以充分接触,提高原料利用率,
故答案为:使反应物充分接触,提高原料利用率;
(2)炼铁时要用到焦炭,它有两个作用.炼铁时需要高温,焦炭与氧气反应生成二氧化碳,同时放出大量热,可供给炼铁使用;炼铁时还需一氧化碳作还原剂,二氧化碳与过量焦炭反应可以生成一氧化碳.燃烧放热,维持炉温,焦炭是烟煤在隔绝空气的条件下,加热到950℃~1 050℃下制得的,现代炼铁在鼓入空气的同时会喷入煤粉,接触面积大,生成一氧化碳,用一氧化碳的热能供给反应温度,减少焦炭用量,降低成本,
故答案为:减少焦炭用量,降低成本;
(3)石灰石除去铁矿石中的SiO2和生成的SO2等杂质,首先是煅烧石灰石生成氧化钙和二氧化碳,CaCO3$\frac{\underline{\;高温\;}}{\;}$CaO+CO2↑,生成的氧化钙分别与铁矿石中的SiO2和生成的SO2等杂质反应,CaO+SiO2$\frac{\underline{\;高温\;}}{\;}$CaSiO3、CaO+SO2$\frac{\underline{\;高温\;}}{\;}$CaSO3,生成炉渣,
故答案为:CaCO3$\frac{\underline{\;高温\;}}{\;}$CaO+CO2↑、CaO+SiO2$\frac{\underline{\;高温\;}}{\;}$CaSiO3、CaO+SO2$\frac{\underline{\;高温\;}}{\;}$CaSO3.
点评 本题考查炼铁,掌握炼铁的原理是解答关键,题目难度不大.


 高中必刷题系列答案
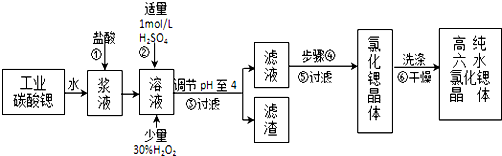
高中必刷题系列答案科目:高中化学 来源: 题型:实验题
| 氢氧化物 | Fe(OH)3 | Fe(OH)2 |
| 开始沉淀的pH | 1.5 | 6.5 |
| 沉淀完全的pH | 3.7 | 9.7 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①②③④ | B. | ②③④① | C. | ②①③④ | D. | ④②③① |
查看答案和解析>>
科目:高中化学 来源: 题型:推断题

查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 氨水稀释后,溶液中$\frac{c(N{H}_{4}^{+})}{c(N{H}_{3}•{H}_{2}O)}$的值减小 | |
| B. | 0.1 mol•L-1Na2CO3溶液加蒸馏水稀释,CO32-的水解程度增大,溶液的pH减小 | |
| C. | 电解精炼铜过程中,阳极质量的减少与阴极质量的增加一定相等 | |
| D. | 298 K时,2H2S(g)+SO2(g)═3S(s)+2H2O(l)能自发进行,则其△H<0 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
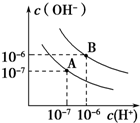 已知水在25℃和95℃时,其电离平衡曲线如图所示:
已知水在25℃和95℃时,其电离平衡曲线如图所示:查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 可用聚氯乙烯代替乙烯制作食品包装袋 | |
| B. | 去除银器表面Ag2S,可将银器放在盛有食醋的铝锅中煮沸片刻 | |
| C. | 开发核能、太阳能等新能源,推广甲醇汽油,使用无磷洗涤剂都符合环保理念 | |
| D. | “连续纤维增韧”航空材料主要是由碳化硅、陶瓷和碳纤维复合而成,是一种新型无机非金属材料 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com