
【题目】向一定量 CO2 和 NaOH 溶液反应后的某溶液中逐滴滴入稀盐酸,开始阶段未产生 CO2气体,则该溶液中的溶质组成可能是_____________。
 同步练习河南大学出版社系列答案
同步练习河南大学出版社系列答案 同步练习西南师范大学出版社系列答案
同步练习西南师范大学出版社系列答案 补充习题江苏系列答案
补充习题江苏系列答案 学练快车道口算心算速算天天练系列答案
学练快车道口算心算速算天天练系列答案科目:高中化学 来源: 题型:
【题目】A是相对分子质量为28的烃。以A为原料合成有机化合物D的方法如下图所示。

(1)A→B的反应类型是_______。
(2)B→C反应的试剂及条件是_______。
(3)C→D反应的化学方程式是_______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氢气是未来非常理想的能源,科学家最近研制出利用太阳能产生激光,并在二氧化钛(TiO2)表面作用使海水分解得到氢气的新技术:2H2O![]() 2H2+O2。制得的氢气可用于燃料电池、合成氨工业。回答下列问题:
2H2+O2。制得的氢气可用于燃料电池、合成氨工业。回答下列问题:
(1)分解海水时,________能转变为________能。生成的氢气用于燃料电池时,________能转变为________能。
(2)某种氢氧燃料电池是用NaOH溶液作电解质,正极的电极反应式为________;若把燃料改为甲烷,负极的电极反应式为________。
(3)氢气可用于合成氨。一定温度下,向2L 的密闭容器中加入1 molN2和 3molH2发生反应 N2(g)+3H2(g)![]() 2NH3(g),2min时测得N2的浓度为0.3mol/L,5min时达到平衡,此时测得压强为开始时的
2NH3(g),2min时测得N2的浓度为0.3mol/L,5min时达到平衡,此时测得压强为开始时的![]() 。则前2min用NH3表示的化学反应速率为________;平衡时,N2的转化率为________,混合气体的平均相对分子质量为________。
。则前2min用NH3表示的化学反应速率为________;平衡时,N2的转化率为________,混合气体的平均相对分子质量为________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】N2和H2在催化剂表面合成氨的微观历程及能量变化的示意图如下,用![]() 、
、![]() 、
、![]() 分别表示N2、H2、NH3,下列说法正确的是
分别表示N2、H2、NH3,下列说法正确的是

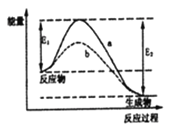
A. 使用催化剂,合成氨反应放出的热量减少
B. 在该过程中,N2、H2断键形成N原子和H原子
C. 在该过程中,N原子和H原子形成了含有非极性键的NH3
D. 合成氨反应中,反应物断键吸收能量大于生成物形成新键释放的能量
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】天津是我国研发和生产锂离子电池的重要基地。锂离子电池正极材料是含锂的二氧化钴(LiCoO2),充电时LiCoO2中Li被氧化,Li+迁移并以原子形式嵌入电池负极材料碳(C6)中,以LiC6表示。电池反应为LiCoO2+ C6![]() CoO2+ LiC6,下列说法正确的是
CoO2+ LiC6,下列说法正确的是
A. 充电时,电池的负极反应为 LiC6- e-="=" Li + C6
B. 放电时,电池的正极反应为 CoO2+ Li++ e-="=" LiCoO2
C. 羧酸、醇等含活泼氢的有机物可用作锂离子电池的电解质
D. 锂离子电池的比能量(单位质量释放的能量)低
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一种磁性材料的磨削废料(含镍质量分数约21%)主要成分是铁镍合金,还含有铜、钙、镁、硅的氧化物。由该废料制备纯度较高的氢氧化镍,工艺流程如下:
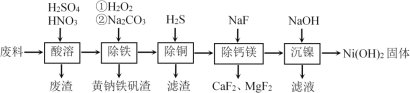
回答下列问题:
(1)合金中的镍难溶于稀硫酸,“酸溶”时除了加入稀硫酸,还要边搅拌边缓慢加入稀硝酸,反应有N2生成。写出金属镍溶解的离子方程式________________________。
(2)“除铁”时H2O2的作用是____________________,为了证明添加的H2O2已足量,应选择的试剂是____________________(填“铁氰化钾”或“硫氰化钾”)溶液。黄钠铁矾[NaxFey(SO4)m(OH)n]具有沉淀颗粒大、沉淀速率快、容易过滤等特点,则x∶y∶m∶n=1∶3∶2∶________。
(3)“除铜”时,反应的离子方程式为_________________________,若用Na2S或Na2S2O3代替H2S除铜,优点是__________________________。
(4)已知除杂过程在陶瓷容器中进行,NaF的实际用量为理论用量的1.1倍,用量不宜过大的原因是_______________________________。
(5)100kg废料经上述工艺制得Ni(OH)2固体的质量为31kg,则镍回收率的计算式为_______。
(6)镍氢电池已成为混合动力汽车的主要电池类型,其工作原理如下:M+Ni(OH)2![]() HM+NiOOH(式中M为储氢合金)。写出电池放电过程中正极的电极反应式________。
HM+NiOOH(式中M为储氢合金)。写出电池放电过程中正极的电极反应式________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图为某蛋白质的结构示意图,其中“—S—S—”为由两个“—SH”脱氢形成的二硫键,其作用是连接两个相邻肽链。若该蛋白质分子共由m个氨基酸组成,则形成一个该蛋白质分子时生成的水分子数和减少的相对分子质量分别为

A. m,18m
B. (m-4),18(m-4)
C. (m-3),18(m-3)+4
D. (m-2),18(m-2)+4
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】硼氢化钠(NaBH4)在有机合成、化工生产方面有广泛应用。制备硼氢化钠的化学方程式为NaBO2+2SiO2+4Na+2H2![]() NaBH4+2Na2SiO3。下列有关上述反应的说法错误的是( )
NaBH4+2Na2SiO3。下列有关上述反应的说法错误的是( )
A. 氧化产物和还原产物的物质的量之比为2:1
B. 转移4 mol电子时,只需向装置中通入44.8 L H2(标准状况)
C. 装药品之前加热装置至100℃并持续一会儿
D. 制备硼氢化钠的副产物可能有NaH
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】W、X、Y、Z四种短周期元素,它们在周期表中位置如图所示,这4种元素的原子最外层电子数之和为23,下列说法不正确的是
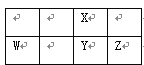
A. W、Y、X三种元素的原于半径依次减小
B. X元素的简单气态氢化物的沸点比Y的高
C. W元素与氢元素可能会形成W2H6
D. Y元素的单质能从NaZ溶液中置换出Z元素的单质
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com