
分析 根据V=$\frac{m}{ρ}$计算出硝酸钙溶液的体积,再根据n=$\frac{m}{M}$计算出4g硝酸钙的物质的量,结合硝酸钙的化学式计算出溶液中硝酸根离子的物质的量,最后根据c(NO3-)=$\frac{n}{V}$计算出硝酸根离子的物质的量浓度.
解答 解:该硝酸钙溶液的体积为:V=$\frac{40g}{pg/mL}$=$\frac{40}{p}$mL,
4g硝酸钙的物质的量为:$\frac{4g}{164g/mol}$=$\frac{1}{41}$mol,则该硝酸钙溶液中含有硝酸根离子的物质的量为:$\frac{1}{41}$mol×2=$\frac{2}{41}$mol,
则该溶液中硝酸根离子的物质的量浓度为:c(NO3-)=$\frac{\frac{2}{41}mol}{\frac{40}{p}×1{0}^{-3}L}$=$\frac{50p}{41}$mol•L-1,
故答案为:$\frac{50p}{41}$.
点评 本题考查了物质的量浓度的计算,题目难度不大,明确物质的量浓度的概念及表达式为解答关键,注意掌握物质的量与摩尔质量、物质的量浓度之间的关系.


 芝麻开花课程新体验系列答案
芝麻开花课程新体验系列答案 怎样学好牛津英语系列答案
怎样学好牛津英语系列答案科目:高中化学 来源: 题型:解答题
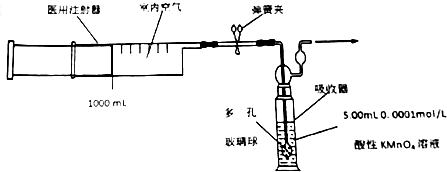
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | X-衍射实验可以区分晶体和非晶体 | B. | SiO2属于原子晶体 | ||
| C. | 金属钋是简单立方堆积 | D. | 晶格能的大小只与离子半径有关 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
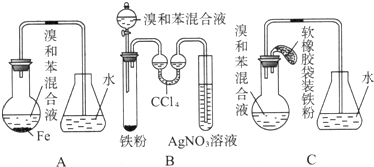
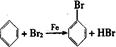 、2Fe+3Br2=2FeBr3;写出B的试管中还发生的反应化学方程式HBr+AgNO3=AgBr↓+HNO3
、2Fe+3Br2=2FeBr3;写出B的试管中还发生的反应化学方程式HBr+AgNO3=AgBr↓+HNO3查看答案和解析>>
科目:高中化学 来源: 题型:解答题
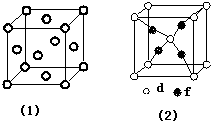 周期表前四周期的元素a、b、c、d、e、f,原子序数依次增大.a是宇宙中最丰富的元素,b的某种核素在考古时用来测定一些文物的年代,d与e同族,用e氧化物漂白的草帽日久又变成黄色;f的最外层只有1个电子,但次外层有18个电子.回答下列问题;
周期表前四周期的元素a、b、c、d、e、f,原子序数依次增大.a是宇宙中最丰富的元素,b的某种核素在考古时用来测定一些文物的年代,d与e同族,用e氧化物漂白的草帽日久又变成黄色;f的最外层只有1个电子,但次外层有18个电子.回答下列问题;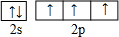 ,f在周期表中的位置是第四周期第IB族
,f在周期表中的位置是第四周期第IB族 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 己烷、己烯和CCl4可以用溴水鉴别 | |
| B. | 除去甲苯中的苯乙烯(C6H5CH═CH2)可以用溴水 | |
| C. | 乙烯、聚氯乙烯和苯分子中均含有碳碳双键 | |
| D. | 乙烯和二氧化硫使溴水褪色的原理相同 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com