
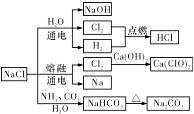
 NaCI是一种化工原料,可以制备一系 列物质(如图所示),下列说法正确的是( )
NaCI是一种化工原料,可以制备一系 列物质(如图所示),下列说法正确的是( )| A. | 常温干燥的Cl2能用钢瓶储存,所以Cl2不与铁反应 | |
| B. | 工业上利用澄清石灰水与Cl2反应来制漂白粉 | |
| C. | 往NaCl溶液中先通足量氨气后,再通入足量CO2才可能析出NaHCO3 | |
| D. | 电解含酚酞的NaCl溶液,由于OH-往阳极移动,故阳极先变红 |
分析 A、铁能在氯气中燃烧生成棕黄色的烟FeCl3;
B、工业上利用氯气和石灰乳反应来制取漂白粉;
C、NH3极易溶于水,而CO2在水中的溶解度不大,据此分析;
D、电解NaCl溶液,阳极上Cl-放电,阴极上来自于水的H+放电,故OH-在阴极生成.
解答 解:A、常温下,铁与干燥的氯气不反应,但在点燃的条件下两者能反应:3Cl2+2Fe$\frac{\underline{\;点燃\;}}{\;}$2FeCl3,故A错误;
B、由于Ca(OH)2的水溶性较差,在水中的溶解度不大,故工业上利用氯气和石灰乳反应来制取漂白粉,而不是利用氯气和澄清石灰水反应来制取漂白粉,故B错误;
C、NH3极易溶于水,而CO2在水中的溶解度不大,故应先向饱和NaC1溶液中通入足量NH3,再通入足量CO2,可析出NaHCO3晶体,故C正确;
D、电解NaCl溶液,阳极上Cl-放电,阴极上来自于水的H+放电,故OH-在阴极生成,故阴极先变红,故D错误.
故选C.
点评 本题综合考查了铁与氯气的反应条件、漂白粉的制取、侯氏制碱法和电解饱和食盐水中两极上的离子放电情况,难度不大,掌握好基础是解题关键.


科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 乙醇和甲醇 | B. | 邻羟基苯甲醛与对羟基苯甲醛 | ||
| C. | 对羟基苯甲酸与邻羟基苯甲酸 | D. | H2O和H2S |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
| 乙醇 | 溴乙烷 | 正丁醇 | 1-溴丁烷 | |
| 密度/g•cm-3 | 0.7893 | 1.4604 | 0.8098 | 1.2758 |
| 沸点/℃ | 78.5 | 38.4 | 117.2 | 101.6 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
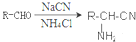 ,②
,②
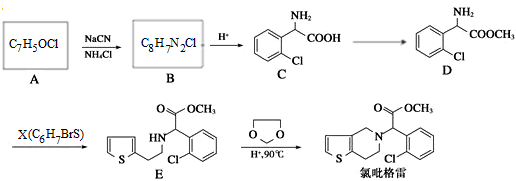
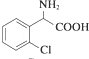 +CH3OH $→_{△}^{浓硫酸}$
+CH3OH $→_{△}^{浓硫酸}$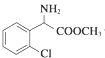 +H2O,反应类型取代反应.
+H2O,反应类型取代反应.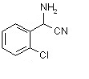 ,X
,X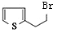 .
.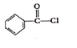 .
. .
.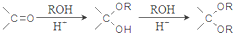 ,设计一条由乙烯、甲醇为有机原料制备化合物
,设计一条由乙烯、甲醇为有机原料制备化合物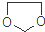 的合成路线流程图,无机试剂任选.(合成路线常用的表反应试剂A反应条件B…反应试剂反应条件目标产物示方式为:A$→_{反应条件}^{反应试剂}$B…$→_{反应条件}^{反应试剂}$目标产物)
的合成路线流程图,无机试剂任选.(合成路线常用的表反应试剂A反应条件B…反应试剂反应条件目标产物示方式为:A$→_{反应条件}^{反应试剂}$B…$→_{反应条件}^{反应试剂}$目标产物)查看答案和解析>>
科目:高中化学 来源: 题型:解答题
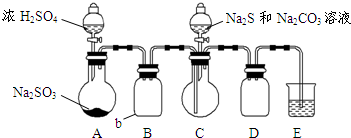 硫代硫酸钠是一种重要的化工产品.某兴趣小组拟制备硫代硫酸钠晶体(Na2S2O3•5H2O).
硫代硫酸钠是一种重要的化工产品.某兴趣小组拟制备硫代硫酸钠晶体(Na2S2O3•5H2O).查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 硝酸体积(mL) | 100 | 200 | 300 | 400 |
| 剩余固体(g) | 18.0 | 9.6 | 0 | 0 |
| 放出气体的体积(mL) | 2240 | 4480 | 6720 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com