
分析 (1)依据燃烧热概念是1mol可燃物完全燃烧生成稳定氧化物放出的热量,题干所给量计算32g甲醇燃烧生成二氧化碳和液态水放热,结合热化学方程式书写方法,标注物质聚集状态和对应焓变;
(2)根据热化学方程式的书写方法结合热化学方程式的意义来回答;
(3)利用盖斯定律,将②×2+③-①即得到反应④,反应热为△H=2△H2+△H3-△H1,以此解答;
(4)根据混合气体的体积计算混合气体的物质的量,结合气体体积比计算甲烷、氢气的物质的量,再根据热化学反应方程式计算放出的热量.
解答 解:(1)在25℃、101kPa下,1g甲醇(CH3OH)燃烧生成CO2和液态水时放热22.68kJ.32g甲醇燃烧生成二氧化碳和液态水放出热量为725.76KJ;则表示甲醇燃烧热的热化学方程式为:CH3OH(l)+$\frac{3}{2}$O2(g)=CO2(g)+2H2O(l)△H=-725.76kJ•mol-1,
故答案为:CH3OH(l)+$\frac{3}{2}$O2(g)=CO2(g)+2H2O(l)△H=-725.76kJ•mol-1;
(2)适量的N2和O2完全反应,每生成23克NO2需要吸收16.95kJ热量,所以每生成92克NO2需要吸收67.8kJ热量,则热化学方程式为:N2(g)+2O2(g)=2NO2(g)△H=67.8kJ•mol-1,
故答案为:N2(g)+2O2(g)=2NO2(g)△H=67.8kJ•mol-1;
(3)①C2H2(g)+$\frac{5}{2}$O2(g)═2CO2(g)+H2O(l)△H1=-1301.0kJ•mol-1
②C(s)+O2(g)═CO2(g)△H2=-393.5kJ•mol-1
③H2(g)+$\frac{1}{2}$O2(g)═H2O(1)△H3=-285.8kJ•mol-1,
根据盖斯定律可知,②×2+③-①即得到反应④2C(s)+H2(g)═C2H2(g),所以该反应的△H=-393.5 kJ•mol-1×2-285.8 kJ•mol-1+1301.0 kJ•mol-1=+228.2 kJ•mol-1,
故答案为:+228.2 KJ/mol;
(4)甲烷和氢气的混合气体11.2L(已折合成标准状况),所以甲烷和氢气的混合气体的总的物质的量为0.5mol,
甲烷和氢气的体积比为4:1,所以甲烷的物质的量为0.5mol×$\frac{4}{5}$=0.4mol,氢气的物质的量为0.5mol-0.4mol=0.1mol.
由CH4(g)+2O2(g)═CO2(g)+2H2O(l)△H=-Q1kJ/mol可知,
0.4mol甲烷燃烧放出的热量为0.4mol×Q1kJ/mol=0.4Q1kJ;
由2H2(g)+O2(g)═2H2O(l)△H=-Q3kJ/mol可知,
0.1mol氢气燃烧生成液态水放出的热量为0.1mol×$\frac{1}{2}$×Q3kJ/mol=0.05Q3kJ,
所以放出的热量为0.4Q1+0.05Q3,
故答案为:0.4Q1+0.05Q3kJ.
点评 本题考查反应热的计算、盖斯定律的应用、热化学方程式的书写等,题目难度不大,注意第(4)题中根据水的状态选择相应的热化学方程式计算反应热.


科目:高中化学 来源: 题型:选择题
| A. | ⑤①②③④⑥⑦ | B. | ③⑤①②⑥⑦④ | C. | ③⑤②⑦①⑥④ | D. | ②⑥⑦①③⑤④ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 热化学方程式中,化学式前面的化学计量数既可表示微粒数,又可表示物质的量 | |
| B. | 热化学方程式中,如果没有注明温度和压强则表示在标准状况下测得的数据 | |
| C. | 书写热化学方程式时,不仅要写明反应热的符号和数值,还要注明各物质的聚集状态 | |
| D. | 1mol碳燃烧所放出的热量为燃烧热,1mol强酸和1mol强碱完全反应所放出的热称为中和热 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | AgCl的溶解度增大 | B. | AgCl的溶解度、溶度积KSP均不变 | ||
| C. | AgCl的溶度积KSP增大 | D. | AgCl的溶解度、溶度积KSP均增大 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 温度/℃ | 200 | 300 | 400 |
| K | 1.0 | 0.86 | 0.5 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 物质的溶解性为难溶,则该物质的溶解度为0 | |
| B. | 某离子被沉淀完全是指该离子在溶液中的浓度为0 | |
| C. | 通过沉淀反应能将大部分杂质离子沉淀 | |
| D. | 难溶电解质的溶度积越小,溶解度越大 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
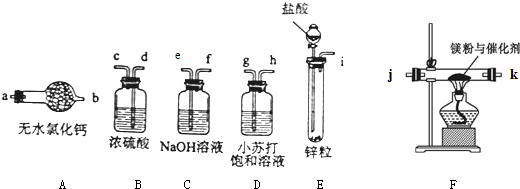
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com