
【题目】海洋中有丰富的食品、矿产、能源和药物.如图是从海水中提取某些原料的流程图. 
下列有关说法正确的是( )
A.第①步中除去粗盐中的SO42﹣、Ca2+、Mg2+、Fe3+等杂质,加入的药品顺序为:Na2CO3溶液→NaOH溶液→BaCl2溶液→过滤后加盐酸
B.工业上通过氯碱工业制取金属钠
C.从第③步到第⑤步的目的是浓缩、富集溴单质
D.第②步的反应条件是高温加热
科目:高中化学 来源: 题型:
【题目】在硫酸工业生产中,为了有利于SO2的转化,且能充分利用热能,采用了中间有热交换器的接触室(见图).下列说法错误的是( ) 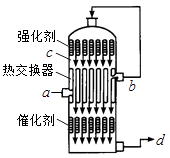
A.a、b两处的混合气体成分含量相同,温度不同
B.c、d两处的混合气体成分含量相同,温度不同
C.热交换器的作用是预热待反应的气体,冷却反应后的气体
D.c处气体经热交换后再次催化氧化的目的是提高SO2的转化率
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是( )
A. 原子最外层电子数为2的元素一定处于周期表IIA族
B. 原子序数相差2的两元素不可能处于同一主族
C. 可根据氢化物的稳定性和酸性强弱,来判断非金属元素得电子能力强弱
D. 非金属元素的最高化合价不超过其元素电子的最外层电子数
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列反应的离子方程式书写正确的是( )
A.氢氧化钡溶液与稀 H2SO4 反应:Ba2++SO ![]() +H++OH﹣═BaSO4↓+H2O
+H++OH﹣═BaSO4↓+H2O
B.稀 H2SO4与铁粉反应:2Fe+6H+═2Fe3++3H2↑
C.硝酸银溶液与铁粉反应:2Ag++Fe═Fe2++2Ag
D.碳酸钙与盐酸反应:CO ![]() +2H+═H2O+CO2↑
+2H+═H2O+CO2↑
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关物质的制备和转化正确的是
A.常温下,用铝与浓硫酸反应制备二氧化硫
B.氯化钡溶液中通入二氧化硫可生成BaSO3沉淀
C.用FeS除去废水中的重金属铜离子
D.以粗铜作阴极,硫酸铜溶液为电解质溶液电解精炼铜
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关说法正确的是( )
A. 原子的最外层有两个电子的元素都在第ⅡA族
B. 第ⅠA族元素都是典型的金属元素
C. 氟、氯、氧、氮四种元素都是第ⅦA族的元素
D. 第三周期的元素的原子核外都有三个电子层
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列反应方程式书写正确的是( )
A.甲醛和足量银氨溶液充分反应:HCHO+2Ag(NH3)2++2O﹣ ![]() ?HCOO﹣+NH4++2Ag↓+H2O+3NH3
?HCOO﹣+NH4++2Ag↓+H2O+3NH3
B.往苯酚钠溶液中通入少量二氧化碳气体: ![]()
C.向盛有硫酸铜水溶液的试管里加入过量氨水:Cu2++4NH3?H2O═[Cu(NH3)4]2++4H2O
D.溴乙烷中滴入AgNO3溶液检验其中的溴元素:Br﹣+Ag+═AgBr↓
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】起固定氮作用的化学反应是( )
A. N2与H2在一定条件下反应生成NH3B. 硝酸工厂用NH3氧化制NO
C. NO与O2反应生成NO2D. 由NH3制碳酸氢铵和硫酸铵
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化合物H是合成抗心律失常药物泰达隆的一种中间体,可通过以下方法合成: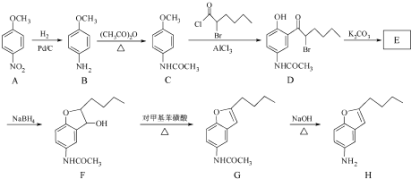
(1)D中的含氧官能团名称为(写两种).
(2)F→G的反应类型为 .
(3)写出同时满足下列条件的C的一种同分异构体的结构简式 .
①能发生银镜反应;
②能发生水解反应,其水解产物之一能与FeCl3溶液发生显色反应;
③分子中只有4种不同化学环境的氢.
(4)E经还原得到F,E的分子是为C14H17O3N,写出E的结构简式 .
(5)已知:①苯胺( ![]() )易被氧化
)易被氧化 ![]() 请以甲苯和(CH3CO)2O为原料制备
请以甲苯和(CH3CO)2O为原料制备 ![]() ,写出制备的合成路线流程图(无机试剂任用,合成路线流程图示例见本题题干).
,写出制备的合成路线流程图(无机试剂任用,合成路线流程图示例见本题题干).
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com