
现有以下6种说法:①氯水、氨水、水玻璃、水银都是混合物;②明矾、冰醋酸、石膏都是电解质;③氯酸、烧碱、纯碱依次分别为酸、碱、盐;④11H+、21H+、31H+互为同位素;⑤胶体带电是电泳的前提条件;⑥生活中常见的石英玻璃、普通玻璃、钢化玻璃都属于硅酸盐产品。其中不正确的是
A.①⑤ B.①④⑤⑥ C.②③④ D.②⑤⑥
科目:高中化学 来源:2017届湖北省老河口市高三10月月考化学卷(解析版) 题型:选择题
下列条件下,可以大量共存的离子组是( )
A.某无色溶液中:Na+、Cu2+、Cl-、MnO4-
B.含有大量Fe3+的溶液中:Na+、SO42-、K+、SCN- -
C.含有大量NH4+的溶液中:Ba2+、 K+、Cl-、OH-
D.在pH=1的溶液中:K+、Fe3+、Cl-、NO3-
查看答案和解析>>
科目:高中化学 来源:2017届福建省高三上联考一化学卷(解析版) 题型:实验题
纳米级Fe粉是新型材料,具有超强磁性、高效催化性。某化学小组探究用氢气和碳酸亚铁制取纳米级铁粉。其实验设计如图(加热、支持装置省略):
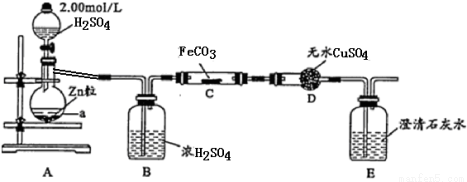
(1)a的名称是________________;浓硫酸的作用是________________。
(2)打开分液漏斗活塞,一段时间后再对C装置加热,这样操作的目的是_______________;反应一段时间后D中变蓝,E中溶液变浑浊,C中发生反应的化学方程式为______________。
(3)反应中若观察到B装置中气泡产生过快,则应进行的操作是_____________________。
(4)反应一段时间后,B中产生气泡太慢,再滴加硫酸,反应速率略有加快但不明显;若向硫酸中加少量硫酸铜,再滴入硫酸与Zn反应,反应速率明显加快,原因是__________________。
(5)检验碳酸亚铁中含有铁元素的实验方法是____________________________。
查看答案和解析>>
科目:高中化学 来源:2017届安徽省六校教育研究会高三上第一次联考化学卷(解析版) 题型:填空题
硫酸及其盐在工农业生产中有着重要的应用。
(1)SO2催化氧化为SO3的反应是工业制硫酸的重要过程,①下图是反应过程中SO2和SO3的浓度隨时间t的变化情况。反应从开始到达到平衡时,用O2表示的平均反应速率为 。
②在一容积可变的密闭容器中充入一定量SO2(g)和O2(g),O2的平衡转化率如图所示。则p1与p2的大小关系是p1 p2 (填“>”“<”或“=”);A、B、C三点的平衡常数大小关系为 (用Ka、Kb、Kc表示三点对应的平衡常数)。

(2)生产硫酸过程中产生的尾气,可用氨水吸收,溶液中生成(NH4)2SO4、(NH4)2SO3等溶质。
①(NH4)2SO4溶液呈酸性的原因是 (用离子方程式表示)。
②己知:
NH3·H2O | H2SO3 | |
电离平衡常数 | 1.7×10—5 | Ka1=1.54×10—2 Ka2=1.02×10—7 |
NH4HSO3溶液呈 (填“酸性”、“碱性”、“中性”)。
③25℃时,相同物质的量的SO2与NH3溶于水,所得溶液中c(H+)—c(OH—)= (填序号)。
A.c(SO32—)—c(H2SO3)
B.c(HSO3—)+c(SO32—)—c(NH4+)
C.c(SO32—)+c(NH3·H2O)—c(H2SO3)
D.(HSO3—)+2c(SO32—)—c(NH4+)
(3)己知:①BaSO4(s)+4C(s)=BaS(s)+4CO(g) △H=+571.2kJ•mo1—1
②BaS(s)=Ba(s)+S(s) △H=+460kJ•mo1—1
③2C(s)+O2(g)=2CO(g) △H=—221kJ•mo1—1
则用Ba(s)、S(s)、O2(g)反应生成BaSO4(s)的热化学方程式为 。
查看答案和解析>>
科目:高中化学 来源:2017届安徽省六校教育研究会高三上第一次联考化学卷(解析版) 题型:选择题
下列说法正确的是
A.—定温度下,将浓度为0.1mol·L—1HF溶液加水不断稀释过程中,电离度和Ka(HF)保持不变,c(F—)/c(HF)始终保持增大
B.浓度均为0.1mol·L—1的Na2SO3、NaHSO3混合溶液中:
3c(Na+)=2[c(SO32—)+c(HSO3—)+c(H2SO3)]
C.在0.1mol·L—1氨水中滴加0.1mol·L—1盐酸,恰好完全中和时pH=a,则由水电离产生的c(OH—) =10—amol·L—1
D.己知:Ksp(AgCl)=1.8×10—10,Ksp(Ag2Cr2O4)=2.0×10—12,则Ag2CrO4的溶解度小于AgCl
查看答案和解析>>
科目:高中化学 来源:2017届安徽省六校教育研究会高三上第一次联考化学卷(解析版) 题型:选择题
NA代表阿伏加德罗常数的数值,下列说法正确的是
A.46g14CO2含有的中子数为22NA
B.标准状况下,22.4LCH3C1含有的分子数为NA
C.lmol甲醇中含有C—H键的数目为4NA
D.6.8g液态KHSO4中含有0.1NA个阳离子
查看答案和解析>>
科目:高中化学 来源:2017届安徽省江淮十校高三11月质检化学试卷(解析版) 题型:填空题
过氧化物和高铁酸盐是工业常用漂白剂,也是重要的工业原料。回答下列问题
(1)过氧作钙不溶于水,但易溶于稀酸。广泛用作胃药,治疗胃酸过多。试写出过氧化盖与胃酸
反应的离子方程式: 。
高温下,过氧化钠在隔绝空气环境中可以将铁单质氧化成FeO42—高铁酸盐和钠的另一种氧化物,该反应的化学方程式为 。常温下,Na2FeO4具有净水功能,反应可生成红褐色难溶物和助燃气体,请写出离子方程式: 。
(2)某小组同学对Na2FeO4作净水剂时,所得到还原产物进行探究并提出假设:
假设①为Fe2+;假设②为Fe3+;假设③为 ;
若假设③成立,请设计实验验证(限选试剂:NaOH溶液、KSCN溶液、H2O2溶液、KMnO4溶液、HNO3溶液、H2SO4溶液;仪器任选)
步骤 | 方案 | 现象 | 结论 |
Ⅰ | 取反应后的溶液分别装于A、B试管中 | ||
Ⅱ | |||
Ⅲ |
查看答案和解析>>
科目:高中化学 来源:2017届安徽省江淮十校高三11月质检化学试卷(解析版) 题型:选择题
化学与生活密切相关,下列叙述正确的是
A.石灰水喷涂在树干上可以消灭树皮上的过冬才虫卵,是因为Ca(OH)2有毒,可毒死虫卵
B.明矾和氯水是常用的水处理剂,常用于海水的淡化
C.侯德榜制碱法先通入NH3是为了增大CO2的溶解度
D.在食品袋中放入盛有CaCl2·6H2O和铁粉透气小袋,可防止食物受潮、氧化变质
查看答案和解析>>
科目:高中化学 来源:2016-2017学年陕西省高二上期中化学卷(解析版) 题型:选择题
下列说法正确的是( )
A.某物质的溶液中由水电离出的c(H+)=1×10-a mol/L,若a>7时,则该溶液的pH一定为14-a
B.相同物质的量浓度的下列溶液中,①NH4Al(SO4)2、②NH4Cl、③CH3COONH4、④NH3·H2O;c(NH4+) 由大到小的顺序是:①>②>③>④
C.物质的量浓度相等的H2S和NaHS混合溶液中:c(Na+)+c(H+)=c(S2-)+c(HS-)+c(OH-)
D.AgCl悬浊液中存在平衡: AgCl(s)  Ag+(aq)+Cl-(aq),往其中加入少量 NaCl粉末,平衡会向左移动,溶液中离子的总浓度会减小
Ag+(aq)+Cl-(aq),往其中加入少量 NaCl粉末,平衡会向左移动,溶液中离子的总浓度会减小
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com