
| 混合物成分 | 提纯所用试剂的化学式 | 离子方程式 |
| (a)MgO中混有少量Al2O3杂质 | ||
| (b)NaHCO3溶液中混有少量Na2CO3 |
分析 (1)在铝与氢氧化钠溶液反应中,实质是铝和水发生氧化还原反应,水得电子,所以氧化剂是水,根据得失电子守恒2Al~~3H2,进行计算求解;
(2)(a)Al2O3能与强碱反应生成偏铝酸根;
(b)通入二氧化碳气体通入二氧化碳生成碳酸氢钠;
(3)制备胶体的原理是利用铁离子水解生成氢氧化铁胶体,反应的离子方程式为Fe3++3H2O=Fe(OH)3(胶体)+3H+,故答案为:Fe3++3H2O=Fe(OH)3(胶体)+3H+;
解答 解:(1)在铝与氢氧化钠溶液反应中,实质是铝和水发生氧化还原反应,水得电子,所以氧化剂是水,
根据得失电子守恒2Al~~3H2~~~~~~转移电子数为:6mol,
54g 3×22.4L 6NA
5.4g V N
所以$\frac{54g}{5.4g}=\frac{3×22.4L}{V}=\frac{6{N}_{A}}{N}$
解之得:V=6.72L,N=0.6NA,故答案为:H2O;6.72;0.6NA;
(2)(a)Al2O3能与强碱反应生成偏铝酸根,反应的离子方程式为Al2O3+2OH-=2AlO2-+H2O;故答案为:NaOH,Al2O3+2OH-=2AlO2-+H2O;
(b)通入二氧化碳气体通入二氧化碳生成碳酸氢钠,反应的离子方程式为;CO32-+CO2+H2O=2 HCO3-;故答案为:CO2,CO32-+CO2+H2O=2 HCO3-;
(3)制备胶体的原理是利用铁离子水解生成氢氧化铁胶体,反应的离子方程式为Fe3++3H2O=Fe(OH)3(胶体)+3H+,故答案为:Fe3++3H2O=Fe(OH)3(胶体)+3H+.
点评 本题考查物质的分离、提纯,侧重于学生的分析能力、实验能力和评价能力的考查,难度不大,注意把握物质的性质的异同,注意除杂时不能引入新的杂质.


 小学能力测试卷系列答案
小学能力测试卷系列答案科目:高中化学 来源: 题型:选择题
| A. | 少量金属钠保存在乙醇中 | |
| B. | 新制氯水存放在带玻璃塞的无色细口瓶中 | |
| C. | 氢氧化钠固体保存在带橡胶塞的广口瓶中 | |
| D. | 浓硝酸保存在带橡胶塞的无色玻璃瓶中 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 溶液的pH:Na2CO3>NaHCO3>CH3COOH>NaHSO4 | |
| B. | 由水电离出的c(H+):Na2CO3>NaHCO3>NaHSO4>CH3COOH | |
| C. | 溶液中的c(NH4+):(NH4)2SO4>(NH4)2CO3>NH4HSO4>NH4Cl | |
| D. | 溶液的pH:(NH4)2CO3>(NH4)2SO4>NH4Cl>NH4HSO4 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①②④ | B. | ① | C. | ③ | D. | ①④ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
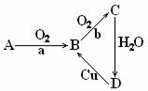

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 3:1 | B. | 2:1 | C. | 1:1 | D. | 1:4 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com