
| A. | 硫酸钡 | B. | 蔗糖 | C. | 醋酸 | D. | 二氧化硫 |
分析 在水溶液中完全电离的电解质为强电解质,在水溶液中部分电离的电解质为弱电解质,可见强弱电解质的根本区别为在溶液中能够完全电离,据此进行解答.
解答 解:A.硫酸钡难溶于水,但溶解的硫酸钡在水溶液中完全电离,属于强电解质,故A错误;
B.蔗糖不导电,在水溶液中也不导电,蔗糖为非电解质,故B错误;
C.醋酸在水溶液中只能部分电离出醋酸根离子和氢离子,所以醋酸为弱电解质,故C正确;
D.二氧化硫是非电解质,故D错误;
故选C.
点评 本题考查了电解质与非电解质、强电解质与弱电解质的判断,题目难度不大,注意明确电解质与非电解质、强电解质与弱电解质的概念及区别,明确单质和混合物不属于电解质、非电解质.


 暑假作业海燕出版社系列答案
暑假作业海燕出版社系列答案科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
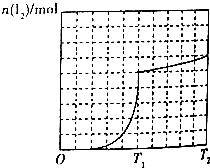 H2O2与KI的酸性溶液反应生成I2的物质的量与温度的关系如图所示(0-T1,T1~T2所用时间相等),下列有关说法正确的是( )
H2O2与KI的酸性溶液反应生成I2的物质的量与温度的关系如图所示(0-T1,T1~T2所用时间相等),下列有关说法正确的是( )| A. | 由于温度升高,反应速率加快,所以T1~T2时段生成I2的反应速率大于0~T1时段 | |
| B. | 由于H2O2分解速率加快,浓度快速减小,所以T℃后升温,生成I2的反应速率变小 | |
| C. | 由上述反应原理可知不能用H2O2除去KCl溶液中少量的HI杂质 | |
| D. | 由图象可知该反应正向为放热反应& |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 煤的气化和液化过程都有化学变化 | |
| B. | 防腐剂福尔马林(含甲醛)可用作食品保鲜剂 | |
| C. | 用碘酒滴加在阿斯匹林、去痛片等药片上,可检验药片是否含有淀粉 | |
| D. | 用浸泡过高锰酸钾溶液的硅藻土吸收水果产生的乙烯以达到保鲜的目的 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | ${\;}_{78}^{202}$Pt的相对原子质量为202 | |
| B. | ${\;}_{78}^{202}$Pt的质子数为202 | |
| C. | 铂元素的质量数为202 | |
| D. | ${\;}_{78}^{202}$Pt的原子核内有124个中子 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 化学键 | H-H | C-H | C≡C |
| 键能/kJ•mol-1 | a | b | c |
| A. | (b-c-a)kJ•mol-1 | B. | (c+3a-4b)kJ•mol-1 | C. | (6b-c-3a)kJ•mol-1 | D. | (c+3a-6b)kJ•mol-1 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com