
| A、在平衡常数的表达式中,反应物用起始浓度,生成物用平衡浓度 |
| B、在任何条件下,一个化学反应的平衡常数都不会改变 |
| C、平衡常数的大小仅跟温度有关,与浓度、压强、催化剂等无关 |
| D、平衡常数越大,化学反应速率越快 |


科目:高中化学 来源: 题型:
| NaCl |
| NH4Cl |
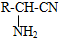 ,R-CN
,R-CN| H+ |

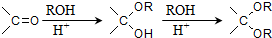 ,写出由乙烯、甲醇为有机原料制备化合物
,写出由乙烯、甲醇为有机原料制备化合物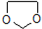 的合成路线流程图(无机试剂任选).合成路线流程图示例如图:CH3CH2OH
的合成路线流程图(无机试剂任选).合成路线流程图示例如图:CH3CH2OH| 浓硫酸 |
| 170℃ |
| Br2 |
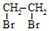
查看答案和解析>>
科目:高中化学 来源: 题型:
| 滴定次数 | 待测溶液体积(mL) | 标准酸体积 | |
| 滴定前的刻度(mL) | 滴定后的刻度(mL) | ||
| 第一次 | 10.00 | 0.40 | 20.50 |
| 第二次 | 10.00 | 4.10 | 24.00 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、Na2O2晶体中阴离子和阳离子 | ||
| B、NaHSO4晶体中阳离子和阴离子 | ||
C、
| ||
| D、氯化钠中的质子总数和电子总数 |
查看答案和解析>>
科目:高中化学 来源: 题型:
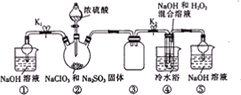 已知亚铝酸钠(NaClO2)为白色粉末,易溶于水,NaClO2饱和溶液在温度低于38℃时析出的晶体是NaClO2
已知亚铝酸钠(NaClO2)为白色粉末,易溶于水,NaClO2饱和溶液在温度低于38℃时析出的晶体是NaClO2查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、上层为紫色液体,下层为无色液体 |
| B、上层为无色液体,下层为紫色液体 |
| C、上层为橙色液体,下层为紫色液体 |
| D、不分层,均为紫色液体 |
查看答案和解析>>
科目:高中化学 来源: 题型:
 正丁醛是一种化工原料.某实验小组利用如下装置合成正丁醛.发生的反应如下:
正丁醛是一种化工原料.某实验小组利用如下装置合成正丁醛.发生的反应如下:| Na2Cr2O7 |
| △H2SO4 |
| 沸点/℃ | 密度/g?cm-3 | 水中溶解性 | |
| 正丁醇 | 117.2 | 0.8109 | 微溶 |
| 正丁醛 | 75.7 | 0.8017 | 微溶 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com