
常温下,浓度均为0.10 mol/L、体积均为V0的HA和HB溶液,分别加水稀释至体积V,pH随 的变化如图所示,下列叙述正确的是( )
的变化如图所示,下列叙述正确的是( )

A.该温度下HB的电离平衡常数约等于1.11×10-5
B.相同条件下NaA溶液的pH大于NaB溶液的pH
C.溶液中水的电离程度:a=c>b
D.当 时,若两溶液同时升高温度,则
时,若两溶液同时升高温度,则 减小
减小
科目:高中化学 来源:2015-2016学年黑龙江双鸭山一中高二下期中化学试卷(解析版) 题型:选择题
化合物A(C4H8Br2)可由下列反应制得,C4H10O C4H8
C4H8 C4H8Br2,则A的结构式不可能的是( )
C4H8Br2,则A的结构式不可能的是( )
A.CH3CH2CHBrCH2Br B.CH3CH(CH2Br)2
C.CH3CHBrCHBrCH3 D.(CH3)2CBrCH2Br
查看答案和解析>>
科目:高中化学 来源:2016届海南省高三高考考前模拟十二化学试卷(解析版) 题型:实验题
某化工厂以天然气、水、空气为基本原料联合生产氨、硝酸,获得了良好的经济效益,下面是其生产流程图。
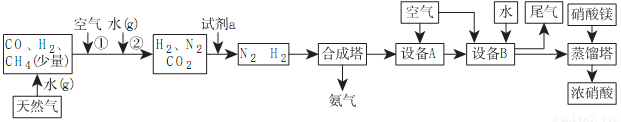
(1)试剂a可能是________,设备B的名称为_________,设备A中的化学方程式为____________。
(2)该化工厂合成氨时的压强40MPa,温度为500℃左右,在此条件下,测定达到平衡时混合气体中NH3的体积分数约为35.2%。
①在保持温度、压强不变的情况下,写出一种能提高合成塔中H2转化率的方法____________,温度越低,NH3的产率越高,为何不在较低温度下进行合成____________。
②从合成塔中出来的NH3的体积分数通常约为15%,其原因是____________。
(3)从设备B中出来的硝酸浓度较小,通常先加入一定量的硝酸镁后再进行蒸馏
①下列可以代替硝酸镁加入到蒸馏塔中的是:____________
A.浓硫酸B.硫酸镁C.生石灰
②蒸馏时通常采用减压蒸馏,这样做的主要目的是____________。
(4)用尿素[CO(NH2)2]处理尾气时可得到纯净的两种常见无毒气体,反应过程为:NO、NO2在水中反应转化亚硝酸,然后亚硝酸再与尿素反应,写出后者反应的化学方程式:____________。
查看答案和解析>>
科目:高中化学 来源:2016届海南省高三高考考前模拟十二化学试卷(解析版) 题型:选择题
某溶液中可能含有物质的量浓度相等的下列离子中的几种:Fe3+、Cu2+、Na+、SO42-、CO32-、NO3-、Cl-、I-,取上述溶液少量分别进行如下实验:①一份中加入少量锌粉后,固体溶解、溶液颜色有变化,但无其它现象产生②一份加入BaCl2溶液后得到白色沉淀,下列有关判断正确的是( )
A.溶液中只含Fe3+、SO42-、Cl-
B.溶液中只含Cu2+、SO42-
C.需要利用焰色反应才能确定有无Na+
D.溶液中肯定没有I-,但无法确定有无Cl-
查看答案和解析>>
科目:高中化学 来源:2016届江西省、临川二中高三下联考理综化学试卷(解析版) 题型:填空题
氧元素和卤族元素都能形成多种物质,我们可以利用所学物质结构与性质的相关知识去认识和理解。
(1)溴的价电子排布式为 ;PCl3的空间构型为
(2)已知CsICl2不稳定,受热易分解,倾向于生成晶格能更大的物质,则它按下列 式发生。
A. CsICl2=CsCl+ICl B. CsICl2=CsI+Cl2
(3)根据下表提供的第一电离能数据判断:最有可能生成较稳定的单核阳离子的卤素原子是___________。
氟 | 氯 | 溴 | 碘 | |
第一电离能(kJ•mol﹣1) | 1681 | 1251 | 1140 | 1008 |
(4)下列分子既不存在s﹣pσ键,也不存在p﹣pπ键的是
A. HCl B.HF C. SO2 D. SCl2
(5)已知COCl2为平面形,则COCl2中心碳原子的杂化轨道类型为 ,写出CO的等电子体的微粒 (写出1个)。
(6)钙在氧气中燃烧时得到一种钙的氧化物晶体,其结构如图所示:由此可判断该钙的氧化物的化学式为 .已知该氧化物的密度是ρg•cm﹣3,则晶胞离得最近的两个钙离子间的距离为 cm(只要求列算式,不必计算出数值,阿伏加德罗常数为NA)。

查看答案和解析>>
科目:高中化学 来源:2016届江西省、临川二中高三下联考理综化学试卷(解析版) 题型:选择题
设NA为阿伏加德罗常数的值。下列说法正确的是( )
A.25℃时,50 g 98%浓硫酸和50 g 98%浓磷酸混合后含氧原子数为4NA
B.28 g聚乙烯中含有的碳原子数为2n NA
C.常温常压下,0.2 g D216O中含有的质子数、中子数和电子数均为0.1NA
D.6.8 g KHSO4晶体中含有0.1 NA个阳离子
查看答案和解析>>
科目:高中化学 来源:2016届福建省高三下学期周考五理科综合化学试卷(解析版) 题型:选择题
乙醛酸(HOOC-CHO)是有机合成的重要中间体.工业上用“双极室成对电解法”生产乙醛酸,原理如图所示.该装置中阴、阳两极为惰性电极,两极室均可产生乙醛酸,其中乙二醛与M电极的产物反应生成乙醛酸.下列说法不正确的是( )

A.N电极上的电极反应式:HOOC-COOH+2e-+2H+═HOOC-CH0+H2O
C.M电极上的电极反应式为:2Cl--2e-═Cl2↑
B.若有2molH+通过质子交换膜并完全参与反应,则该装置中生成的乙醛酸为1mol
D.乙二醛与M电极的产物反应生成乙醛酸的化学方程式:Cl2+OHC-CHO+H2O═HOOC-CHO+2HCl
查看答案和解析>>
科目:高中化学 来源:2016届安徽省六安市高三下综合训练十理综化学试卷(解析版) 题型:选择题
设NA为阿伏加罗常数的值,下列说法正确的是( )
A.3.1g由白磷和红磷组成的混合物中含有磷原子的数目为0.1NA
B.0.1mol丙烯醛中含有双键的数目为0.1NA
C.标准状况下,2.24L乙醇中含有的分子数目为0.1NA
D.1molNaHSO4固体中阳离子的数目为2NA
查看答案和解析>>
科目:高中化学 来源:2015-2016学年贵州省高二下期中化学试卷(解析版) 题型:选择题
短周期元素X、Y、Z、W、Q在元素周期表中的相对位置如下图所示。下列说法正确的是( )
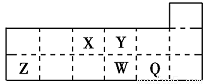
A.元素X与元素Z的最高正化合价之和的数值等于8
B.原子半径的大小顺序为:rX>rY>rZ>rW>rQ。
C.Y2-和Z3+的核外电子数和电子层数都不相同
D.元素W的最高价氧化物对应的水化物的酸性比Q的强
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com