
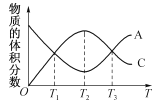
【题目】向密闭容器中充入物质A和B,发生反应aA(g)+bB(g) ![]() cC(g)。反应过程中,物质A的体积分数和C的体积分数随温度(T)的变化曲线如图所示。下列说法正确的是
cC(g)。反应过程中,物质A的体积分数和C的体积分数随温度(T)的变化曲线如图所示。下列说法正确的是
A.该反应在T1、T3温度时达到化学平衡 B.该反应在T2温度时达到化学平衡
C.该反应的逆反应是放热反应 D.升高温度,平衡会向正反应方向移动
【答案】B
【解析】
试题分析:T2℃之前A%变小,C%从0渐增大,而T2℃之后A%渐大,C%渐小,说明T2℃之前是反应没有达到平衡状态,而T2℃时恰好平衡,T2℃之后是温度升高使平衡向左移动,所以逆反应是吸热反应。A、T1温度之后A%继续变小,C%继续增大,T3温度之后A%继续增大,C%继续减小,故T1、T3温度时未达到化学平衡,A错误;B、T2℃之前A%变小,C%从0渐增大,而T2℃之后A%渐大,C%渐小,说明T2℃时反应达到平衡状态,B正确;C、T2℃时恰好平衡,T2℃之后A%渐大,C%渐小,说明T2℃之后是温度升高使平衡向左移动,所以逆反应是吸热反应,C错误;D、T2℃时恰好平衡,T2℃之后A%渐大,C%渐小,说明T2℃之后是温度升高使平衡向逆反应移动,D错误。答案选B。


科目:高中化学 来源: 题型:
【题目】区别下列有关物质的描述不正确的是( )
A.用氢氧化钠溶液区别乙醇溶液和乙酸
B.用金属钠区别无水乙醇和苯
C.用碳酸钠溶液区别乙酸和乙酸乙酯
D.用溴水区别甲烷和乙烯
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】根据所学知识,请回答下列问题:
(1)用离子方程式表示除去铁粉中混有的铝粉 。
(2)检测Fe2(SO4)3溶液中是否含有少量的FeSO4的操作方法是__________________。
(3)用H2O2和稀H2SO4的混合溶液可溶出印刷电路板金属粉末中的铜,请写出表示该过程的离子方程式 。
(4)工业制备粗硅的化学方程式 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】向100mL0.1mol·L-1硫酸亚铁铵[(NH4)2Fe(SO4)2]溶液中逐滴滴入0.1mol·L-1Ba(OH)2溶液。随着Ba(OH)2溶液体积V的变化,沉淀总物质的量n的变化如下图所示。则下列说法中正确的是

A. a点时溶液中所含主要溶质为(NH4)2SO4
B. a→b段发生反应的离子方程式是 SO![]() +Ba2+===BaSO4↓
+Ba2+===BaSO4↓
C. b点为最大沉淀量,对应的纵坐标值为0.02
D. c点加入Ba(OH)2溶液的体积为200 mL
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法或推理正确的是
A. 将Fe(N03)2样品溶于稀H2SO4后,滴加KSCN溶液,溶液变红,则Fe(N03)2晶体已氧化变质
B. 常温下,pH都为11的氢氧化钠溶液和氨水均加水稀释100倍,pH都变为9
C. 25℃时,Ksp(BaCO3)>Ksp(BaCrO4),则沉淀水体中的Ba2+选择Na2CrO4比Na2CO3好
D. 将CH3CH2Br与NaOH溶液共热,冷却后取出上层溶液,加入AgNO3溶液,产生沉淀,则CH3CH2Br在NaOH溶液中发生了水解
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(10分)醇酸树脂容易固化成膜,成膜后有光泽和韧性,附着力强,井具有良好的耐磨性和绝缘性等性能,下面是一种醇酸树脂M的合成路线:

已知:①有机物C的核磁共振氢谱显示只有两种不同化学环境的氢
②
按要求回答问题:
(1)F中官能团的名称为_______,已知条件中②的反应类型为_______
(2)B的结构简式为_______。
(3)写出C+F→M的化学方程式:_______。
(4)符合下列条件的 同分异构体有______种。
同分异构体有______种。
A.能与浓溴水反应产生白色沉淀,且1mol该物质可消耗2molBr2
b.能发生消去反应
(5)设计以甲醛和丙醛为原料制备![]() 的合成路线(用流程图表示,无机试剂任选)注:合成路线的书写格式参照如下实例:
的合成路线(用流程图表示,无机试剂任选)注:合成路线的书写格式参照如下实例:
![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如表是元素周期表的一部分,按要求填空( 填元素符号或化学式):
族 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
2 | ① | ② | ③ | ④ | ||||
3 | ⑤ | ⑥ | ⑦ | ⑧ | ⑨ | ⑩ |
(1)写出①元素的元素名称 .
(2)写出⑩元素的元素符号 .
(3)⑨在元素周期表中的位置:第 周期,第 族.
(4)在这些元素中, 是最活泼的金属元素; 是最活泼的非金属元素; 是最不活泼的元素.(用元素符号填写)
(5)能形成气态氢化物,且气态氢化物最稳定的是 .(用化学式填写)
(6)这些元素的最高价氧化物对应水化物中最强的酸是 ;最强的碱是 ;具有两性的氢氧化物是 .(用化学式填写)
(7)从⑤到的元素中, 原子半径最小.(用元素符号填写)
(8)比较⑤与⑥的化学性质, 更活泼(用元素符号填写),试用实验证明此现象(简述实验操作、现象和结论) .
(9)用电子式表示元素④与⑥形成的化合物: ,该化合物属于 (填“共价”或“离子”)化合物.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】过氧乙酸(CH3COOOH)是一种高效消毒剂,具有很强的氧化性和腐蚀性,可以迅速杀灭多种微生物,包括多种病毒(如SARS 病毒)、细菌、真菌及芽孢。过氧乙酸可由冰酸酸与过氧化氢在一定条件下作用制得,下列有关过氧乙酸的叙述中正确的是
A.过氧乙酸与羟基乙酸(HOCH2COOH)互为同分异构体
B.过氧乙酸与苯酚混合使用,可增强过氧乙酸的杀菌效果
C.由下列过氧乙酸的制取原理可以看出,过氧乙酸是酯的同系物
CH3COOH+H-O-O-H→![]() +H2O
+H2O
D.浓过氧乙酸溶液中加入少许紫色石蕊试液,一定呈红色
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com