
【题目】实验室用乙醇和浓硫酸反应制备乙烯,化学方程式为:C2H5OH![]() CH2=CH2↑+H2O,接着再用液溴与乙烯反应制备1,2-二溴乙烷。在制备过程中由于部分乙醇与浓硫酸发生氧化还原反应还会产生CO2、SO2,并进而与Br2反应生成HBr等酸性气体。某学习小组用上述三种为原料,组装下列仪器(短接口或橡皮管均己略去)来制备1,2-二溴乙烷
CH2=CH2↑+H2O,接着再用液溴与乙烯反应制备1,2-二溴乙烷。在制备过程中由于部分乙醇与浓硫酸发生氧化还原反应还会产生CO2、SO2,并进而与Br2反应生成HBr等酸性气体。某学习小组用上述三种为原料,组装下列仪器(短接口或橡皮管均己略去)来制备1,2-二溴乙烷
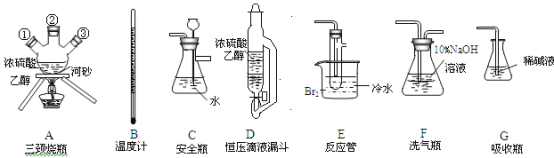
(1)如果气体流向从左到右,正确的连接顺序是:
B经A①插入A中,D接入②;A③接__接__接___接___。
(2)温度计水银球的正确位置是_________。
(3)装置D与分流漏斗相比,其主要优点是_______。
(4)装置C的主要作用是_______,装置F的作用是__________。
(5)在反应管E中进行的主要反应的化学方程式为________。
(6)装置E烧杯中的泠水和反应管内液溴上的水层作用均是_______________。若将装置F拆除,在E中的主要反应为_______。
【答案】C F E G 位于三颈瓶的液体中央 平衡上下压强,使液体顺利滴下 防倒吸 除去三颈瓶中产生的CO2、SO2,吸收挥发的溴蒸汽 CH2=CH2+ Br2![]() BrCH2CH2Br 减少溴的挥发 SO2+Br2+2H2O=H2SO4+2HBr
BrCH2CH2Br 减少溴的挥发 SO2+Br2+2H2O=H2SO4+2HBr
【解析】
(1)根据装置中试剂可知ABD用来制备乙烯,由于生成的乙烯中含有SO2和CO2等气体,在利用乙烯与溴反应之前需要除去。C起到安全瓶的作用,目的是为防止倒吸。E装置用来制备1,2—二溴乙烷,生成的1,2—二溴乙烷中含有溴,利用F装置除杂,最后利用G装置进行尾气处理,则正确的连接顺序是B经A①插入A中,D接入②;A③接C、F、E、G。
(2)温度计测量的是溶液的温度,因此位于三颈瓶的液体中央;
(3)D是恒压漏斗,能保持内外压强相同,则其作用是平衡上下压强,使液体顺利滴下;
(4)根据以上分析可知装置C的主要作用是防倒吸。装置F的作用是除去三颈瓶中产生的CO2、SO2并吸收挥发的溴蒸汽;
(5)E装置用来制备1,2—二溴乙烷,反应的方程式为CH2=CH2+ Br2![]() BrCH2CH2Br。
BrCH2CH2Br。
(6)由于液溴易挥发,则装置E烧杯中的冷水和反应管内液溴上的水层作用均是减少溴的挥发;若将装置F拆除,则SO2易与溴发生氧化还原反应,所以在E中的主要反应为SO2+Br2+2H2O=H2SO4+2HBr。


科目:高中化学 来源: 题型:
【题目】写出下列反应的化学方程式,并指出反应类型。
(1)溴苯的制备_________________________________________________(_____________)。
(2)用甲苯制备TNT _____________________________________________(_____________)。
(3)由丙烯制备聚丙烯____________________________________________(_____________)。
(4)溴乙烷与氢氧化钠的乙醇溶液加热______________________________(_____________)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】弱电解质的电离平衡、盐类的水解平衡和难溶物的溶解平衡均属于化学平衡。根据要求回答问題。
(1)生活中明矾常作净水剂,其净水的原理是_____________(用离子方程式表示)。
(2)常温下,取0.2 mol/L HCl溶液与0.2mol/L MOH溶液等体积混合,测得混合后溶液的pH=5,则PH=13的MOH溶液的浓度_______0.1mol/L(填<、>或=)。
(3)0.1mol/L的NaHA溶液,测得溶液显碱性。则
① 该溶液中 c(H2A)_______________c(A2-)(填<、>或=)。
② 作出上述判断的依据是_____________(用文字解释)。
(4)含Cr2O72-的废水毒性较大,某工厂废水中含5.0×10-3 mol/L的Cr2O72-。为了使废水的排放达标,进行如下处理:
![]()
绿矾为FeSO4 7H2O。反应(I)中Cr2O72-与FeSO4的物质的量之比为___________。常温下若处理后的废水中c(Cr3+)=6.0×10-7mol/L,则处理后的废水的 pH=_______。{Ksp[Cr(OH)3]=6.0×10-31}
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】镁一空气电池的工作原理如图所示,电池反应为Mg+O2+2H2O=2Mg(OH)2。下列有关该电池的说法不正确的是(已知阴离子交换膜的作用是只允许阴离子通过)( )
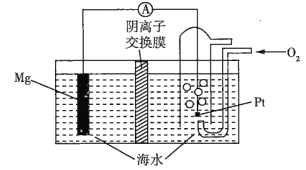
A.通入氧气的电极为正极
B.放电时,溶液中的OH-移向负极
C.负极的电极反应式为Mg-2e-+2OH-=Mg(OH)2
D.当电路中转移0.04mol电子时,参加反应的O2为0.02mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】对于反应N2O4(g)![]() 2NO2(g)在温度一定时,平衡体系中NO2的体积分数φ(NO2)随压强的变化情况如图所示(实线上的任何一点为对应压强下的平衡点),下列说法正确的是
2NO2(g)在温度一定时,平衡体系中NO2的体积分数φ(NO2)随压强的变化情况如图所示(实线上的任何一点为对应压强下的平衡点),下列说法正确的是
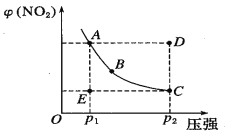
A. A、C两点的正反应速率的关系为A>C
B. A、B、C、D、E各状态中,v(正)<v(逆)的是状态E
C. 维持P1不变,E→A所需时间为x;维持P2不变,D→C所需时间为y,则x<y
D. 使E状态从水平方向到达C状态,从理论上来讲可选用的条件是从P1突然加压至P2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某温度下,pH=11的氨水和NaOH溶液分别加水稀释100倍,溶液的pH随溶液体积变化的曲线如图所示。根据图像判断错误的是( )
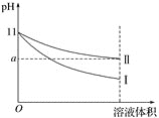
A. a值一定大于9
B. Ⅰ为NaOH溶液稀释时溶液的pH变化曲线
C. 完全中和稀释相同倍数后的两溶液,消耗相同浓度的稀H2SO4的体积V(NaOH)<V(氨水)
D. 稀释后氨水中水的电离程度比NaOH溶液中水的电离程度大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,用AgNO3溶液分别滴定浓度均为0.01mol/L的KCl、K2C2O4溶液,所得的沉淀溶解平衡图象如图所示(不考虑C2O42-的水解)。下列叙述正确的是
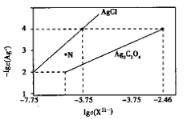
A. Ag2C2O4+2Cl-![]() 2AgCl+C2O42-的平衡常数为109.04
2AgCl+C2O42-的平衡常数为109.04
B. N点表示AgCl的不饱和溶液
C. 向c(Cl-)=c(C2O42-)的混合液中滴入AgNO3溶液时,先生成Ag2C2O4沉淀
D. Ksp(Ag2C2O4)的数量级等于10-7
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学与生活密切相关。下列说法错误的是
A. PM2.5是指粒径不大于2.5μm的可吸入悬浮颗粒物
B. 绿色化学要求从源头上消除或减少生产活动对环境的污染
C. 燃煤中加入CaO可以减少酸雨的形成及温室气体的排放
D. 天然气和液化石油气是我国目前推广使用的清洁燃料
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】可降解高分子材料P的结构为: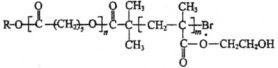 。如图是P的合成路线。
。如图是P的合成路线。

已知:![]() +R3OH
+R3OH![]() +R2OH
+R2OH
(1)B的结构简式是_______,试剂a是_______。
(2)![]() 中官能团的名称是_____、_____。
中官能团的名称是_____、_____。
(3)③的化学方程式是______。
(4)⑥的反应类型是_____。
(5)G与E互为同分异构体,符合下列要求的G共有______种。(不考虑立体异构)
①含有和E(C6H10O3)相同的含氧官能团②分子中含有六元环状内酯结构
(6)当④中反应物以物质的量之比1:1发生反应时,反应⑤的化学方程式是_____。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com