
| A. | NaOH溶液 | B. | 稀硫酸 | C. | 盐酸 | D. | Ba(OH)2溶液 |
分析 根据生成物的化学式:NaAlO2、Al2(SO4)3、AlCl3、Ba(AlO2)2,通过物料守恒可直接判断出等量的铝消耗溶质的物质的量,由此分析解答.
解答 解:设Al为1mol,
A.铝与氢氧化钠溶液反应生成NaAlO2,1molAl消耗1molNaOH;
B.铝与稀硫酸反应生成Al2(SO4)3,1mol铝消耗1.5mol硫酸;
C.铝与盐酸1mol反应生成AlCl3,铝消耗3mol盐酸;
D.铝与Ba(OH)2溶液反应生成Ba(AlO2)2,铝消耗0.5molBa(OH)2,
综合以上分析可知放出氢气且消耗溶质物质的量最少的是Ba(OH)2溶液,
故选D.
点评 本题考查铝的性质,侧重于物质的量的判断,解答时可根据生成物的化学式,从质量守恒的角度分析,题目难度不大.


科目:高中化学 来源: 题型:解答题
 质量相等的C4H6和N2气体在容积可变的容器中的体积和温度的关系如图所示.
质量相等的C4H6和N2气体在容积可变的容器中的体积和温度的关系如图所示.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 3种 | B. | 4种 | C. | 2种 | D. | 5种 |
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
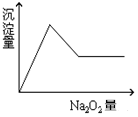 某溶液中可能含有下列8种离子中的一种或几种:H+、Na+、Cu2+、Mg2+、Al3+、NH4+、CO32-、Cl-.向该溶液中加入Na2O2固体放出一种无色无味的气体且产生白色沉淀,沉淀的量随加入Na2O2的量变化关系如图所示.试对该溶液中离子组成情况作出判断.
某溶液中可能含有下列8种离子中的一种或几种:H+、Na+、Cu2+、Mg2+、Al3+、NH4+、CO32-、Cl-.向该溶液中加入Na2O2固体放出一种无色无味的气体且产生白色沉淀,沉淀的量随加入Na2O2的量变化关系如图所示.试对该溶液中离子组成情况作出判断.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 常温常压下,64g SO2气体中所含分子数为NA | |
| B. | 标准状况下,4.48L四氯化碳中所含原子总数为NA | |
| C. | 1mol HNO3作氧化剂时转移电子数为3NA | |
| D. | 常温常压下,11.2L NO2中所含分子数为0.5NA |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 电解精炼粗铜(含有锌铁等杂质),若阳极溶解32g铜,转移电子数目为NA | |
| B. | 256gS8(分子结构如图)含S-S键数为7NA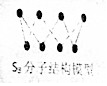 | |
| C. | 某温度下,pH=1的1LH2SO4溶液中含有的H+数目为0.1NA | |
| D. | 氢氧燃料电池正极消耗22.4L气体时,负极消耗的气体分子数目为2NA |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com