
| A. | 增大 | B. | 减小 | C. | 无法判断 | D. | 不变 |
科目:高中化学 来源: 题型:填空题
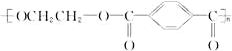
 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | SO2通入酸性高锰酸钾溶液中使之褪色 | |
| B. | SO2通入石蕊试液中使之变红色 | |
| C. | SO2通入氯水中使之褪色 | |
| D. | SO2通入饱和H2S溶液中析出浅黄色沉淀 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Na+、NO3-、Al3+、Cl- | B. | Na+、CO32-、K+、NO3- | ||
| C. | Ca2+、K+、SO42-、Cl- | D. | Fe2+、K+、Cl-、NO3- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 6个碳原子有可能都在一条直线上 | B. | 有5个碳原子可能在一条直线上 | ||
| C. | 6个碳原子一定都在同一平面上 | D. | 6个碳原子不可能在同一平面上 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 物质A和B混合时会发生放热反应.将等物质的量的浓度的A和B溶液,以不同的体积比混合,但总体积始终保持100mL.混合后体系的最高温度如图所示,则A、B两种物质反应时其物质的量的之比是( )
物质A和B混合时会发生放热反应.将等物质的量的浓度的A和B溶液,以不同的体积比混合,但总体积始终保持100mL.混合后体系的最高温度如图所示,则A、B两种物质反应时其物质的量的之比是( )| A. | 1:3 | B. | 3:2 | C. | 3:1 | D. | 4:1 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 三种元素形成的离子半径与原子半径大小顺序相同 | |
| B. | Z是地壳中含量最多的元素 | |
| C. | M、N、R晶体类型相同 | |
| D. | 少量M、N投入水中所得溶液的溶质相同 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
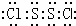 ,属极性分子(填极性或非极性).
,属极性分子(填极性或非极性).查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | S2-的结构示意图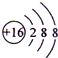 | B. | 乙酸的结构简式:C2H4O2 | ||
| C. | 中子数为20的氯原子:${\;}_{17}^{20}$CL | D. | 二氧化碳分子的比例模型是: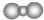 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com