
设NA为阿伏加德罗常数的值,下列叙述正确的是( )
A. pH=1的稀硫酸中含有的H+数为0.1NA
B. 1 mol Na2O和Na2O2混合物中含有的阴、阳离子总数是3NA
C. 50mL 18.4mol/L浓硫酸与足量铜微热反应,生成SO2分子数目为0.46NA
D. 80g NH4NO3晶体中含有NH4+小于个NA
考点: 阿伏加德罗常数.
分析: A、溶液体积不明确;
B、过氧化钠由2个钠离子和1个过氧根构成;
C、铜只能与浓硫酸反应;
D、1molNH4NO3晶体中含1molNH4+.
解答: 解:A、溶液体积不明确,故溶液中的氢离子的个数无法计算,故A错误;
B、过氧化钠由2个钠离子和1个过氧根构成,故1 mol Na2O和Na2O2混合物中含2mol钠离子和1mol阴离子,即3NA个,与Na2O和Na2O2所占的比例无关,故B正确;
C、铜只能与浓硫酸反应,当硫酸变稀后反应即停止,故生成的二氧化硫分子个数小于0.46NA个,故C错误;
D、18gNH4NO3的物质的量为1mol,而1molNH4NO3晶体中含1molNH4+即NA个,故D错误.
故选B.
点评: 本题考查了阿伏伽德罗常数的计算,掌握公式的运用和物质的结构是解题的关键,难度不大.


 名校通行证有效作业系列答案
名校通行证有效作业系列答案科目:高中化学 来源: 题型:
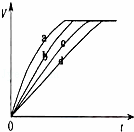
等质量的铁与过量的盐酸在不同的实验条件下进行反应,测定在不同时间(t)产生气体体积(V)的数据,根据数据绘制得到图1,则曲线a、b、c、d所对应的实验组别可能是( )
组别 C(HCL)(mol/L) 温度(℃) 状态
1 2.0 25 块状
2 2.5 30 块状
3 2.5 50 块状
4 2.5 30 粉末状
A. 3﹣4﹣1﹣2 B. 1﹣2﹣4﹣3 C. 4﹣2﹣3﹣1 D. 4﹣3﹣2﹣1
查看答案和解析>>
科目:高中化学 来源: 题型:
氢气是未来最理想的能源,科学家最近研制出利用太阳能产生激光,并在二氧化钛(TiO2)表面作用使海水分解得到氢气的新技术:2H2O 2H2↑+O2↑,制得的氢气可用于燃料电池,试回答下列问题:
2H2↑+O2↑,制得的氢气可用于燃料电池,试回答下列问题:
(1)水分解时,断裂的化学键为 键(填离子或共价),分解海水的反应属于 反应(填放热或吸热).
(2)某种氢氧燃料电池是用固体金属化物陶瓷作电解质,两极上发生的电极反应分别为:A极:2H2+2O2﹣﹣4e﹣═2H2O;B极:O2+4e﹣═2O2﹣则A极是电池的 极;电子从该极 (填流入或流出).
(3)有人以化学反应:2Zn+O2+4H+═2Zn2++2H2O为基础设计一种原电池,移入人体内作为心脏起搏器的能源,它们靠人体内血液中溶有一定浓度的O2、H+、Zn2+进行工作,则原电池的负极发生的电极反应为 .
查看答案和解析>>
科目:高中化学 来源: 题型:
为了提纯下表所列物质(括号内为杂质),有关除杂试剂和分离方法的选择均正确的是( )
选项 被提纯的物质 除杂试剂 分离方法
A 己烷(己烯) 溴水 分液
B 淀粉溶液(NaCl) 水 过滤
C CH3CH2OH(CH3COOH) CaO 蒸馏
D CO2(SO2) Na2CO3溶液 洗气
A. A B. B C. C D. D
查看答案和解析>>
科目:高中化学 来源: 题型:
一种盐与烧碱混合共热,可放出无色气体Y,Y经一系列氧化后的产物再溶于水可得Z溶液,Y和Z溶液反应又可生成X,则盐X是( )
A. (NH4)2SO4 B. NH4NO3 C. NH4Cl D. NH4HCO3
查看答案和解析>>
科目:高中化学 来源: 题型:
CO2与H2的混合气体5g,在150℃时和足量的氧气混合,用电火花充分引燃,在相同状况下再将反应后所得混合气体通入到足量的Na2O2中,测得Na2O2固体增重的质量为3.4g,则原混合气体中CO2的物质的量分数为( )
A. 75% B. 25% C. 88% D. 32%
查看答案和解析>>
科目:高中化学 来源: 题型:
 向绝热恒容密闭容器中通入SO2和NO2,一定条件下使反应SO2(g)+NO2(g)SO3(g)+NO(g)达到平衡,正反应速率随时间变化的示意图如右图所示。由图可得出的正确结论是( )
向绝热恒容密闭容器中通入SO2和NO2,一定条件下使反应SO2(g)+NO2(g)SO3(g)+NO(g)达到平衡,正反应速率随时间变化的示意图如右图所示。由图可得出的正确结论是( )
A.反应在c点达到平衡状态
B.反应物浓度:a点小于b点
C.反应物的总能量低于生成物的总能量
D.Δt1=Δt2时,SO2的转化率:a~b段小于b~c段
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com