
| A. | 乙醛 | B. | 甲醛 | C. | 丙醛 | D. | 丁醛 |
分析 生成Ag的物质的量为:$\frac{21.6g}{108g/mol}$=0.2mol,若为甲醛,则HCHO~4Ag,故HCHO为0.05mol,根据碳元素生成二氧化碳为0.05mol,而等量的醛完全燃烧产生CO2为:$\frac{8.96L}{22.4L/mol}$=0.4mol>0.05mol,故不能为HCHO,根据R-CHO~2Ag计算醛的物质的量,根据碳原子守恒计算醛中C原子数目,饱和一元醛的通式是CnH2nO,进而确定分子式.
解答 解:生成Ag的物质的量为:n(Ag)=$\frac{21.6g}{108g/mol}$=0.2mol,若为甲醛,根据HCHO~4Ag可知HCHO的物质的量为:0.2mol×$\frac{1}{4}$=0.05mol,根据碳元素生成二氧化碳为0.05mol,而等量的醛完全燃烧产生CO2为:$\frac{8.96L}{22.4L/mol}$=0.4mol>0.05mol,则一定不是HCHO,
根据关系式R-CHO~2Ag可知,醛的物质的量为:0.2mol×$\frac{1}{2}$=0.1mol,根据碳原子守恒可知醛中C原子数目为$\frac{0.4mol}{0.1mol}$=4,
所以该饱和一元醛的分子式为C4H8O,为丁醛,
故选D.
点评 本题考查化学方程式计算,题目难度不大,明确反应对应的实质为解答关键,注意银镜反应中甲醛与Ag的比例关系,试题侧重考查学生的分析能力及化学计算能力.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:选择题
| A. | CH3COOCH2CH2CH3 | B. | CH3CH2COOCH2CH3 | ||
| C. | CH3COOCH2CH3 | D. | CH3CH2COOCH2CH=CH2 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA |
| 2 | Li | Be | B | C | N | O | F |
| 3 | Na | Mg | Al | Si | P | S | Cl |
 .
. .
.查看答案和解析>>
科目:高中化学 来源: 题型:实验题
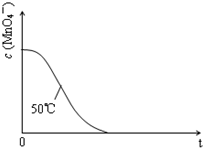 某小组利用H2C2O4溶液和酸性KMnO4溶液反应来探究“条件对化学反应速率的影响”.实验时,先分别量取两种溶液,然后倒入试管中迅速振荡混合均匀,开始计时,通过测定褪色所需时间来判断反应的快慢.该小组设计了如表的方案.
某小组利用H2C2O4溶液和酸性KMnO4溶液反应来探究“条件对化学反应速率的影响”.实验时,先分别量取两种溶液,然后倒入试管中迅速振荡混合均匀,开始计时,通过测定褪色所需时间来判断反应的快慢.该小组设计了如表的方案. | 编号 | H2C2O4溶液 | 酸性KMnO4溶液 | 温度/℃ | ||
| 浓度/mol•L-1 | 体积/mL | 浓度/mol•L-1 | 体积/mL | ||
| ① | 0.10 | 2.0 | 0.010 | 4.0 | 25 |
| ② | 0.20 | 2.0 | 0.010 | 4.0 | 25 |
| ③ | 0.20 | 2.0 | 0.010 | 4.0 | 50 |
查看答案和解析>>
科目:高中化学 来源: 题型:推断题

查看答案和解析>>
科目:高中化学 来源: 题型:推断题
| A | ①能使溴的四氯化碳溶液褪色;②比例模型为 ;③能与水在一定条件下反应生成C ;③能与水在一定条件下反应生成C |
| B | ①由C、H两种元素组成;②球棍模型为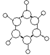 |
| C | ①由C、H、O三种元素组成;②能与Na反应,但不能与NaOH溶液反应;③能与E反应生成相对分子质量为100的酯 |
| D | ①相对分子质量比C少2;②能由C氧化而成 |
| E | ①由C、H、O三种元素组成;②球棍模型为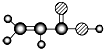 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 碳和水反应吸收131.3kJ 能量 | |
| B. | 1mol 碳和1mol 水反应生成一氧化碳和氢气并吸收131.3kJ 热量 | |
| C. | 1mol 固态碳和1mol 水蒸气反应生成一氧化碳气体和氢气,并吸热131.3kJ | |
| D. | 1 个固态碳原子和1 分子水蒸气反应吸热131.1kJ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com