
 研究NO2、SO2、CO等大气污染气体的处理具有重要意义.
研究NO2、SO2、CO等大气污染气体的处理具有重要意义.| t1~t2 | t3~t4 | t5~t6 | t6~t7 |
| K1 | K2 | K3 | K4 |
分析 (1)利用平衡的特征“等、定”及由此衍生的一些物理量来判断;
(2)升高温度,体系颜色加深,则说明平衡逆向移动,由此判断该反应的△H;
(3)根据压强之比等于物质的量之比计算平衡时混合气体总的物质的量,再利用差量法计算参加反应的二氧化硫的物质的量,结合热化学方程式计算放出的热量;
(4)根据(1)计算可知,原平衡时SO3的体积分数为$\frac{1mol}{4.5mol}$=$\frac{2}{9}$,将起始物质的量改为amol SO2、bmol O2、cmol SO3(g)及固体催化剂,平衡时SO3的体积分数为$\frac{2}{9}$,则与原平衡为等效平衡,计算原平衡时二氧化硫的物质的量,欲使起始时反应表现为向正反应方向进行,则a应大于原平衡状态时二氧化硫的物质的量,结合极限法判断;
(5)假定体积为VL,利用三段式计算原平衡时各组分的物质的量,进而计算平衡常数,将起始物质的量改为3mol SO2、6mol O2、3mol SO3(g)及固体催化剂,计算此时的浓度商,与平衡常数比较判断反应进行方向;
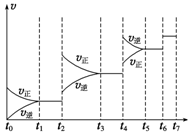
(6)t4时正逆反应速率都较原平衡时的速率大,可升高温度或增大压强;t6时正逆反应速率都较原平衡时的速率大,但平衡不移动,前后气体系数之和不等,只能是使用催化剂;在反应向逆反应之前衡混合物中CO的含量最高;
(7)平衡常数只与温度有关,温度改变平衡常数改变,据此判断.
解答 解:(1)①a.由反应可知,三氧化硫是气体,反应前后气体的物质的量改变,体系压强始终保持不变,不能判定平衡状态,故a错误;
b.混合气体的颜色保持不变,即二氧化氮的浓度不变,达到平衡状态,故b正确;
c.SO2和NO2起始量不等,变化量相等,当SO2和NO2的体积比保持不变,可判断反应达到平衡,故c正确;
d.每生成1 mol SO3的同时消耗1mol NO2,只能判断正反应速率,不能确定正逆反应速率的关系,不能判定平衡状态,故d错误;
e.混合气体的质量和体积始终不变,密度始终是定值,不一定是平衡状态,故e错误;
故答案为:bc;
(2)升高温度,体系颜色加深,说明平衡逆向移动,则该反应的△H<0,故答案为:<;
(3)由题意气体压强为起使时的90%,则反应后总的物质的量为起使时的90%,平衡时总物质的量为(3mol+2mol)×90%=4.5mol,则平衡时各组成物质的量变化为:
2SO2+O2?2SO3 物质的量减少△n
2 1 2 1
1mol 0.5mol 1mol (3mol+2mol)-4.5mol=0.5mol
此时放出的热量为196.6KJ×$\frac{0.5mol}{1mol}$=98.3KJ,
故答案为:98.3kJ;
(4)原平衡时SO3的体积分数为$\frac{1mol}{4.5mol}$=$\frac{2}{9}$,将起始物质的量改为amol SO2、bmol O2、cmol SO3(g)及固体催化剂,平衡时SO3的体积分数为$\frac{2}{9}$,则与原平衡为等效平衡,则a+c=3 b+0.5c=2,由(1)计算可知,平衡时二氧化硫的物质的量为3mol-1mol=2mol,欲使起始时反应表现为向正反应方向进行,则2<a≤3,
故答案为:2<a≤3;
(5)由题意气体压强为起使时的90%,则反应后总的物质的量为起使时的90%,平衡时总物质的量为(3mol+2mol)×90%=4.5mol,则平衡时各组成物质的量变化为:
2SO2+O2?2SO3
开始(mol):3 2 0
变化(mol):1 0.5 1
平衡(mol):2 1.5 1
假定体积为VL,则k=$\frac{(\frac{1}{V})^{2}}{(\frac{2}{V})^{2}×\frac{1.5}{V}}=\frac{V}{6}$,将起始物质的量改为3mol SO2、6mol O2、3mol SO3(g)及固体催化剂,此时的浓度商Qc=$\frac{(\frac{3}{V})^{2}}{(\frac{3}{V})^{2}×\frac{6}{V}}=\frac{V}{6}$,等于平衡常数,处于平衡状态,平衡不移动,
故答案为:不;
(6)t4时正逆反应速率都较原平衡时的速率大,反应向逆反应方向移动,升高温度;t6时正逆反应速率都较原平衡时的速率大,但平衡不移动,前后气体系数之和不等,只能是使用催化剂;在t4时反应向逆反应方向移动,则t3~t4时平衡混合物中CO的含量最高,
故答案为:升高温度;t3~t4;
(7)由图象分析可知,t1~t2与t3~t4温度相同,t5~t6与t7~t8温度相同,且t4后升高温度,平衡逆向移动,平衡常数逆向移动,则k1=k2>k3=k4,
故答案为:k1=k2>k3=k4.
点评 考查反应热的计算、平衡状态的判断、化学平衡影响因素和平衡计算的分析判断,(5)中反应进行方向判断为易错点、难点,综合性较强,掌握基础是关键,题目难度中等.


 唐印文化课时测评系列答案
唐印文化课时测评系列答案 导学与测试系列答案
导学与测试系列答案科目:高中化学 来源: 题型:解答题
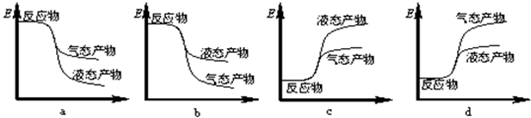
| 2min | 4min | 6min | 8min | … | |
| CO | 0.07 | 0.06 | 0.06 | 0.05 | … |
| H2 | x | 0.12 | 0.12 | 0.2 | … |
| CH3OH | 0.03 | 0.04 | 0.04 | 0.05 | … |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
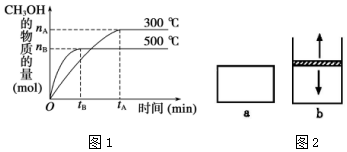 一定条件下,在体积为 3L 的密闭容器中反应 CO(g)+2H2(g)?CH3OH(g)△H=akJ•mol-1,△S=b J•mol-1•K-1(a、b 均为正数),达到化学平衡状态.
一定条件下,在体积为 3L 的密闭容器中反应 CO(g)+2H2(g)?CH3OH(g)△H=akJ•mol-1,△S=b J•mol-1•K-1(a、b 均为正数),达到化学平衡状态.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 CO是火力发电厂释放出的主要尾气,为减少对环境污染,发电厂试图采用CO与Cl2在催化剂的作用下合成光气(COCl2).某温度下,向2L的密闭容器中投入一定量的CO和Cl2,在催化剂的作用下发生反应:CO(g)+Cl2(g)?COCl2(g)△H=a kJ/mol
CO是火力发电厂释放出的主要尾气,为减少对环境污染,发电厂试图采用CO与Cl2在催化剂的作用下合成光气(COCl2).某温度下,向2L的密闭容器中投入一定量的CO和Cl2,在催化剂的作用下发生反应:CO(g)+Cl2(g)?COCl2(g)△H=a kJ/mol| t/min | n (CO)/mol | n (Cl2)/mol |
| 0 | 1.20 | 0.60 |
| 1 | 0.90 | |
| 2 | 0.80 | |
| 4 | 0.20 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 0.1mol/LNaHCO3溶液与0.1mol/LNaOH溶液等体积混合,所得溶液中:c(Na+)>c(HCO3-)>c(OH-)>c(CO32-) | |
| B. | 20ml0.1mol/LCH3COONa溶液与10ml0.1mol/LHCl溶液混合后呈酸性,所得溶液中:c(CH3COO-)>c(Cl-)>c(CH3COOH)>c(H+) | |
| C. | 室温下,pH=2的盐酸与pH=12的氨水等体积混合,所得溶液中:c(NH4+)>c(Cl-)>c(OH-)>c(H+) | |
| D. | 0.1mol/LCH3COOH溶液与0.1mol/LNaOH溶液等体积混合,所得溶液中:c(OH-)>c(H+)+c(CH3COOH) |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 标准状况下,22.4 L H2O中含有氢原子数目为2NA | |
| B. | 17 g NH3所含质子数为10NA | |
| C. | 0.1mol Cu(NO3)2中含有的离子数目为0.2NA | |
| D. | 28g N2 体积为22.4L |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com