
| A. | NH3易液化,液氨常用作制冷剂 | |
| B. | 与金属反应时,稀HNO3可能被还原为更低价态,则稀HNO3氧化性强于浓HNO3 | |
| C. | 氨盐受热易分解,因此贮存氨态氮肥时要密封保存,并放在阴凉通风处 | |
| D. | 稀HNO3和活泼金属反应时不能得到氢气 |
分析 A、氨很容易液化,液态氨汽化时要吸收大量的热,使周围物质的温度急剧下降,所以氨常作为制冷剂;
B、根据与金属反应时的剧烈程度来比较氧化性强弱;
C、根据氨盐的不稳定性;
D、由于硝酸的氧化性,不能得到H2,主要得到NO;
解答 解:A、因NH3易液化,液氨常用作制冷剂,故A正确;
B、与金属反应时,稀HNO3被还原为NO,反应缓慢,浓HNO3被还原为NO2,反应剧烈,所以稀HNO3的氧化性弱于浓
HNO3,故B错误;
C、氨盐受热易分解,因此贮存氨态氮肥时要密封保存,并放在阴凉处,故C正确;
D、由于稀HNO3的强氧化性,与活泼金属反应时不生成氢气,一般生成氮的氧化物,还可以生成硝酸铵,故D正确;
故选B.
点评 本题主要考查了氮元素及其化合物的有关基础知识.注意硝酸与金属反应不产生氢气.


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:选择题
| A | B | C | D | |
| 正极 | Fe | Fe | C | Cu |
| 负极 | Cu | Zn | Fe | Zn |
| 电解质溶液 | HCl | CuSO4 | CuSO4 | FeSO4 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 编号 | 操 作 | 实验现象 |
| ① | 分别在试管A、B中加入 5mL 5% H2O2溶液,各滴入1~2 滴1mol/L FeCl3溶液.待试管中均有适量气泡出现时,将试管A放入盛有5℃左右冷水的烧杯中;将试管B放入盛有40℃左右热水的烧杯中. | 试管A中不再产生气泡;试管B中产生的气泡量增大 |
| ② | 另取两支试管分别加入 5mL 5%H2O2溶液和 5mL10%H2O2溶液. | 试管A、B中均未明显见到有气泡产生 |
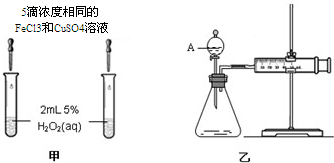
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 苯的分子式为C6H6,它不能使酸性KMnO4溶液褪色,属于饱和烃 | |
| B. | 从苯的结构简式 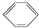 看,苯分子中含有碳碳双键,应属于烯烃 看,苯分子中含有碳碳双键,应属于烯烃 | |
| C. | 在催化剂作用下,苯与液溴反应生成溴苯,发生了加成反应 | |
| D. | 苯分子为平面正六边形结构,6个碳原子之间的化学键完全相同 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 7.8g苯中含有C-C单键数目为0.3NA | |
| B. | 标准状况下,2.24L的CHCl3中含有的C-H键数为0.1NA | |
| C. | 1.4g C2H4和C3H8的混合物中含碳原子数为0.1 NA | |
| D. | 13克溶有乙炔的苯乙烯,其所含的电子数目为7 NA |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 四种常见元素的性质或结构信息如表.试根据信息回答有关问题.
四种常见元素的性质或结构信息如表.试根据信息回答有关问题.| 元素 | A | B | C | D |
| 性质 结构 信息 | 原子核外有两个电子层,最外层有3个未成对的电子 | 原子的M层有1对成对的p电子 | 原子核外电子排布为[Ar]3d104sx,有+1、+2两种常见化合价 | 有两种常见氧化物,其中有一种是冶金工业常用的还原剂 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 乙烯使酸性高锰酸钾溶液褪色 | |
| B. | 苯与溴水混合,反复振荡后溴水层颜色变浅 | |
| C. | 油脂使溴的四氯化碳溶液褪色 | |
| D. | 甲烷与氯气混合,光照一段时间后黄绿色消失 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com