
| A. | 向蒸馏水中加入Na2O,水的电离程度变小 | |
| B. | 向0.1mol•L-1的醋酸溶液中加水稀释后溶液中$\frac{c(C{H}_{3}CO{O}^{-})}{c(C{H}_{3}COOH)•c(O{H}^{-})}$不变 | |
| C. | 向0.1mol•L-1的醋酸溶液中加水稀释后溶液中$\frac{c({H}^{+})}{c(C{H}_{3}CO{O}^{-})}$不变 | |
| D. | 向0.1mol•L-1的醋酸溶液稀释到原体积的10倍后,溶液的PH=2 |
分析 A、向蒸馏水中加入Na2O,得到NaOH,碱会抑制水的电离;
B、向0.1mol•L-1的醋酸溶液中,加水稀释,不会引起Ka、Kw的变化;
C、醋酸是弱电解质,加水稀释醋酸溶液,促进醋酸电离,醋酸电离产生的醋酸根离子和氢离子数目增多浓度减小;
D、0.1mol•L-1的醋酸溶液稀释到原体积的10倍后,促进醋酸电离,溶液的PH<2.
解答 解:A、向蒸馏水中加入Na2O,得到NaOH,碱会抑制水的电离,故A正确;
B、醋酸中,Ka/Kw=$\frac{c(C{H}_{3}CO{O}^{-})}{c(C{H}_{3}COOH)•c(O{H}^{-})}$,只受温度影响,向0.1mol•L-1的醋酸溶液中,加水稀释,不会引起比值的变化,故B正确;
C、无限稀释相当于水,但体积增加,醋酸根离子浓度减小,氢离子浓度基本不变,所以$\frac{c({H}^{+})}{c(C{H}_{3}CO{O}^{-})}$增大,故C错误;
D、0.1mol•L-1的醋酸溶液稀释到原体积的10倍后,促进醋酸电离,溶液的PH<2,故D错误.
故选AB.
点评 本题考查了弱电解质溶液加水稀释过程中离子浓度的变化,注意醋酸电离产生的醋酸根离子和氢离子数目增多浓度减小,题目难度不大.


 口算题天天练系列答案
口算题天天练系列答案科目:高中化学 来源: 题型:实验题
 化学反应中的能量变化,通常主要表现为热量的变化.某实验小组用0.50mol/L NaOH溶液和0.50mol/L硫酸溶液进行中和热的测定.测定中和热的实验装置如图所示:
化学反应中的能量变化,通常主要表现为热量的变化.某实验小组用0.50mol/L NaOH溶液和0.50mol/L硫酸溶液进行中和热的测定.测定中和热的实验装置如图所示:| 实验次数 | 起始温度t1/℃ | 终止温度t2/℃ | ||
| H2SO4 | NaOH | 平均值 | ||
| 1 | 26.2 | 26.0 | 26.1 | 30.1 |
| 2 | 27.0 | 27.4 | 27.2 | 33.3 |
| 3 | 25.9 | 25.9 | 25.9 | 29.8 |
| 4 | 26.4 | 26.2 | 26.3 | 30.4 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题

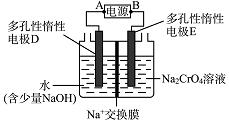
| A. | 甲池中阳离子向通入CH3OH一方的电极区域内移动 | |
| B. | 甲池通入CH3OH的电极反应式为CH3OH-6e-+2H2O═CO32-+8H+ | |
| C. | 反应一段时间后,向乙池中加入一定量Cu(OH)2固体,能使CuSO4溶液恢复到原浓度 | |
| D. | 甲池中消耗280 mL(标准状况下)O2,此时丙池中理论上产生1.45 g固体 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题

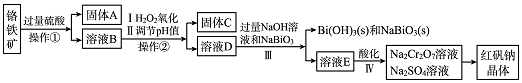
| A. | “吹出”采用热空气而不是常温空气的原因是热空气氧化性强 | |
| B. | 碱液吸收所发生的化学反应中氧化剂与还原剂之比为1:5 | |
| C. | 第③步中“酸化”要用强氧化性的酸,如硝酸 | |
| D. | 含溴的水溶液B中的单质溴浓度比A中的大 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 我国古代四大发明之一黑火药由硫酸、硝酸和木炭按一定比例混合制成 | |
| B. | PH计不能用于酸碱中和滴定终点的判断 | |
| C. | 石油的分馏,煤的干馏、气化、液化均是物理变化 | |
| D. | 可用蘸浓盐酸的棉棒检验输送氨气的管道是否漏气 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
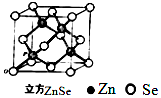 硒化锌是一种透明色半导体,也可作为红光外学材料,熔点1520℃.
硒化锌是一种透明色半导体,也可作为红光外学材料,熔点1520℃.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:解答题
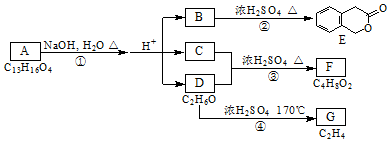
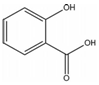 ,其名称为:邻羟基苯甲酸
,其名称为:邻羟基苯甲酸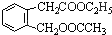 ④反应的反应类型是消去反应
④反应的反应类型是消去反应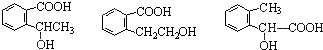 任意一个
任意一个 或CH2=CH2+H2O$\stackrel{催化剂}{→}$CH3CH2OH.
或CH2=CH2+H2O$\stackrel{催化剂}{→}$CH3CH2OH.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com