

| A、sp杂化 |
| B、sp2杂化 |
| C、sp3杂化 |
| D、dsp2杂化 |
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
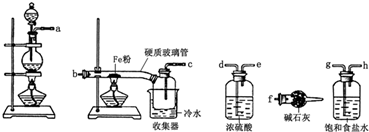
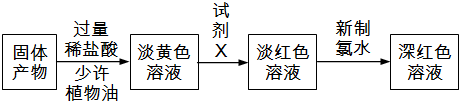
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、①④⑥ | B、①②③④ |
| C、④⑤⑥⑦ | D、全部 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、阴极产物是Cu和H2 |
| B、阳极共产生11.2L的O2 |
| C、电解过程中溶液的PH值不断减小 |
| D、电解过程中电子转移数目4NA |
查看答案和解析>>
科目:高中化学 来源: 题型:
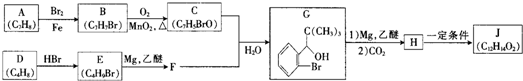

| 反应条件1 |
| 反应条件2 |
| (1)HCHO |
| (2)H2O |
 .
.查看答案和解析>>
科目:高中化学 来源: 题型:
| A、Na2S+2CH3COOH(足量)=2CH3COONa+H2S↑ |
| B、Na2S+2CH3COOH(少量)=2CH3COONa+H2S↑ |
| C、Na2S(少量)+CH3COOH=CH3COONa+NaHS |
| D、CH3COOH+NaHS=CH3COONa+H2S↑ |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A |
| B |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 实验内容 | 实验方法 | 实验现象 |
| 验证氧化性 | ||
| 验证不稳定性 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com