
| A. | 0.5 mol | B. | 0.95 mol | C. | 0.67 mol | D. | 1 mol |
科目:高中化学 来源:2016-2017学年辽宁沈阳东北育才学校高一阶段考一化学卷(解析版) 题型:选择题
NA为阿伏伽德罗常数的值,下列叙述错误的是( )
A.18 g H2O中含的 质子数为10 NA
质子数为10 NA
B.12 g  金刚石含有的电子数为4 NA
金刚石含有的电子数为4 NA
C.46 g NO2和N2O4混合气体中含有原子总数为3 NA
D.23 g Na 与足量 O2反应,生成Na2O和Na2O2的混合物,钠失去NA个电子
查看答案和解析>>
科目:高中化学 来源:2016-2017学年辽宁沈阳东北育才学校高二阶段考一化学卷(解析版) 题型:选择题
在一个密闭容器中发生反应:2SO2(g)+O2(g) 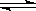 2SO3(g),反应过程中某一时刻SO2、O2、SO3的浓度分别为0.2 mol/L、0.2 mol/L、0.2 mol/L,当反应达到反应限度时可能的数据是( )
2SO3(g),反应过程中某一时刻SO2、O2、SO3的浓度分别为0.2 mol/L、0.2 mol/L、0.2 mol/L,当反应达到反应限度时可能的数据是( )
A.c(SO3)=0.4mol/L
B.c(SO2)=c(SO3)=0.15mol/L
C.c(O2)=0.35mol/L
D.c(SO2)+c(SO3)=0.4mol/L
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 该反应熵判据起决定作用 | B. | 该反应焓判据起决定作用 | ||
| C. | 该反应是熵减的反应 | D. | 该反应是分解反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
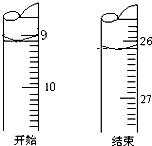 盐酸和氢氧化钠是工业上重要的化工原料,也是实验室里常见的试剂.
盐酸和氢氧化钠是工业上重要的化工原料,也是实验室里常见的试剂.查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 在其他外界条件不变的情况下,使用催化剂,可以改变化学反应进行的方向 | |
| B. | 如果某化学反应的△H和△S均小于0,则反应一定能自发进行 | |
| C. | 化学反应过程中,一定有化学键的断裂和形成 | |
| D. | 反应物的总焓大于生成物的总焓时,△H>0 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:填空题

查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 有关催化机理等问题可从“乙醇催化氧化实验”得到一些认识,实验装置如图所示.其实验操作为:预先使棉花团浸透乙醇,并照图安装好仪器,在铜丝的中间部分加热,片刻后开始有节奏地鼓入空气,即可观察到明显的实验现象.请回答以下问题:
有关催化机理等问题可从“乙醇催化氧化实验”得到一些认识,实验装置如图所示.其实验操作为:预先使棉花团浸透乙醇,并照图安装好仪器,在铜丝的中间部分加热,片刻后开始有节奏地鼓入空气,即可观察到明显的实验现象.请回答以下问题:查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com