


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源:不详 题型:填空题

| 沉淀物 | Fe(OH)3 | Al(OH)3 | Cu(OH)2 |
| 沉淀开始时pH | 2.7 | 4.1 | 8.3 |
| 沉淀完全时pH | 3.7 | 5.4 | 9.8 |
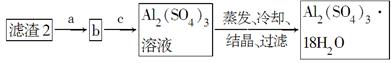
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.Fe在常温下可与浓硝酸、稀硝酸、浓硫酸剧烈反应 |
| B.Al、Cl2均能和NaOH溶液发生氧化还原反应,且两单质的作用相同 |
| C.Na久置于空气中,可以和空气中的有关物质发生反应,最终生成Na2CO3 |
| D.制备FeCl3、CuCl2固体均可采用将溶液直接蒸干的方法 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.浓硫酸具有强氧化性,但SO2气体可以用浓硫酸干燥 |
| B.常温下实验室可以用稀硝酸与铁反应制取NO气体 |
| C.从海水中提取溴的过程中常鼓入热空气,其目的是氧化Br- |
| D.SiO2不仅能与氢氧化钠溶液反应,也能与氢氟酸反应 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.含金属元素的离子一定是阳离子 |
| B.应用蒸馏的方法,可以分离沸点相差较大的液体混合物 |
| C.氯水和过氧化钠都具有漂白作用,其漂白原理相似 |
| D.高炉炼铁时,还原铁矿石的还原剂为一氧化碳 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.①② | B.③④ | C.②④ | D.①③ |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.①②④⑤ | B.②③④⑤ | C.①④⑤ | D.①②③④⑤ |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
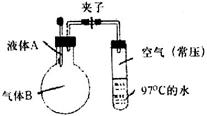
| A.水、氯化氢 | B.硫酸、氨气 |
| C.氢氧化钠溶液、二氧化硫 | D.氢氧化钠溶液、一氧化碳 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| 选项 | 实验操作 | 实验现象 | 结 论 |
| A | 测定等浓度的Na2CO3和Na2SO3 溶液的pH | 前者pH比后者的大 | 非金属性:S>C |
| B | SO2通入酸性高锰酸钾溶液 | 高锰酸钾溶液褪色 | SO2具有还原性 |
| C | 溴乙烷与NaOH溶液共热后,加HNO3酸化的AgNO3溶液 | 出现淡黄色沉淀 | 溴乙烷发生了水解 |
| D | 向等浓度的KBr、KI混合液中滴加AgNO3溶液 | 先出现黄色沉淀 | Ksp(AgBr)>Ksp(AgI) |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com