
��12�֣��й��ܡ�����������������ʼ��±���
�Ȼ��ܿ����ڻ�ѧ��Ӧ����������߸ɼ�����ʪָʾ����ơ����ĭ�ȶ������մ���ɫ������������īˮ�ȡ��ý����ܰ壨������Fe��Ni���Ʊ��Ȼ��ܵĹ����������£�
�������ᷴӦ������������������ſ��ܽ���ʵ��������
��1���������������У�NH3��H2O�����Է�Ӧ���ʵ�Ӱ�죬���±���
�ӱ��п�֪x= ʱ������Ч����á�
��2����������������������һ����ʱ������ɣ�����������в���Co��OH��3���ɣ���д����Ӧ�Ļ�ѧ����ʽ ��
��3���������������м���˫��ˮ������Ӧ�����ӷ���ʽ�� .
��4���������������м���Ĵ��������� ��
��5���ڡ���pH"�����У��������������
��6����֪25��ʱ��Ksp[Fe��OH��3]=4��0��10-38������¶��·�ӦFe3++3H2O![]() Fe��OH��3+3H+��ƽ�ⳣ��Ϊ ��
Fe��OH��3+3H+��ƽ�ⳣ��Ϊ ��

| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| ��ѧʽ | ������ȫʱ��pH | �������� | ||
| Co��OH��2 | 9.4 | Co+2HCl=CoCl2+H2�� Co2++2NH3?H2O=Co��OH��2��+2NH
Ni+2HCl=NiCl2+H2�� Co2++2H2O?Co��OH��2+2H+ Ni2++6NH3?H2O=[Ni��NH3��6]2++6H2O | ||
| Fe��OH��2 | 9.6 | |||
| Fe��OH��3 | 3.7 |

| ��NH3?H2O��PH | ����/% | Ni2+����/% |
| 9 | 98.1 | 0.08 |
| 9.5 | 98 | 0.05 |
| 10 | 97.6 | 0.005 |
| 10.3 | 94 | 0.005 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2011-2012ѧ�꽭��ʡ�����и�����ѧ����ĩ���Ի�ѧ�Ծ� ���ͣ������
��12�֣��й��ܡ�����������������ʼ��±���

�Ȼ��ܿ����ڻ�ѧ��Ӧ����������߸ɼ�����ʪָʾ����ơ����ĭ�ȶ������մ���ɫ������������īˮ�ȡ��ý����ܰ壨������Fe��Ni���Ʊ��Ȼ��ܵĹ����������£�

�������ᷴӦ������������������ſ��ܽ���ʵ��������
��1���������������У�NH3��H2O�����Է�Ӧ���ʵ�Ӱ�죬���±���
�ӱ��п�֪x= ʱ������Ч����á�

��2����������������������һ����ʱ������ɣ�����������в���Co��OH��3���ɣ���д����Ӧ�Ļ�ѧ����ʽ ��
��3���������������м���˫��ˮ������Ӧ�����ӷ���ʽ�� .
��4���������������м���Ĵ��������� ��
��5���ڡ���pH"�����У��������������
��6����֪25��ʱ��Ksp[Fe��OH��3]=4��0��10-38������¶��·�ӦFe3++3H2O Fe��OH��3+3H+��ƽ�ⳣ��Ϊ
��
Fe��OH��3+3H+��ƽ�ⳣ��Ϊ
��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2012�콭��ʡ�����и�����ѧ����ĩ���Ի�ѧ�Ծ� ���ͣ������
��12�֣��й��ܡ�����������������ʼ��±���
�Ȼ��ܿ����ڻ�ѧ��Ӧ����������߸ɼ�����ʪָʾ����ơ����ĭ�ȶ������մ���ɫ������������īˮ�ȡ��ý����ܰ壨������Fe��Ni���Ʊ��Ȼ��ܵĹ����������£�
�������ᷴӦ������������������ſ��ܽ���ʵ��������
��1���������������У�NH3��H2O�����Է�Ӧ���ʵ�Ӱ�죬���±���
�ӱ��п�֪x= ʱ������Ч����á�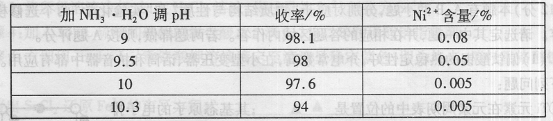
��2����������������������һ����ʱ������ɣ�����������в���Co��OH��3���ɣ���д����Ӧ�Ļ�ѧ����ʽ ��
��3���������������м���˫��ˮ������Ӧ�����ӷ���ʽ�� .
��4���������������м���Ĵ��������� ��
��5���ڡ���pH"�����У��������������
��6����֪25��ʱ��Ksp[Fe��OH��3]=4��0��10-38������¶��·�ӦFe3++3H2O Fe��OH��3+3H+��ƽ�ⳣ��Ϊ ��
Fe��OH��3+3H+��ƽ�ⳣ��Ϊ ��
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com