
| A. | 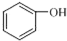 和 和 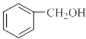 互为同系物 互为同系物 | |
| B. | 乙烷气体中混有乙烯,通入氢气,使乙烯发生加成反应 | |
| C. | 某烃的结构用键线式表示为 ,该烃与Br2按物质的量之比1:1加成时产物有5种 ,该烃与Br2按物质的量之比1:1加成时产物有5种 | |
| D. | 煤经气化和液化两个物理变化过程,可变为清洁能源 |
分析 A.分别为苯酚、苯甲醇;
B.乙烯与氢气发生加成反应,但乙烷中易引入新杂质氢气;
C.烯与溴加成时溴原子连接在相邻的不饱和的C原子上,溴与二烯烃加成可以发生1,2-加成,溴原子连接在相邻的不饱和的C原子上,也可以发生1,4-加成,中间形成1个碳碳双键;
D.煤经气化生成CO和氢气,液化生成甲醇.
解答 解:A.分别为苯酚、苯甲醇,为不同类型的有机物,不是同系物,故A错误;
B.乙烯与氢气发生加成反应,但乙烷中易引入新杂质氢气,应选溴水、洗气除杂,故B错误;
C.当溴与 发生1,2-加成时,生成物有
发生1,2-加成时,生成物有
 、
、 ;
;
当溴与 发生1,4-加成时,生成物有
发生1,4-加成时,生成物有 、
、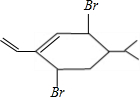 ,显然所得产物有5种,故C正确;
,显然所得产物有5种,故C正确;
D.煤经气化生成CO和氢气,液化生成甲醇,均发生化学变化,故D错误;
故选C.
点评 本题考查有机物的结构与性质,为高频考点,把握官能团与性质的关系、有机反应为解答的关键,侧重分析与应用能力的考查,题目难度不大.


 活力课时同步练习册系列答案
活力课时同步练习册系列答案科目:高中化学 来源: 题型:选择题

| A. | 1mol L分别与足量NaOH溶液和H2反应,最多可消耗4molNaOH和10molH2 | |
| B. | 有机酸M与油酸互为同系物,双酚A与苯酚互为同系物 | |
| C. | 与M含相同官能团的同分异构体还有2种 | |
| D. | 等物质的量的L、A和M 与足量浓溴水发生反应,消耗Br2的量之比为1:2:1 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题

| A. | ②③ | B. | ①② | C. | ③④ | D. | ①④ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
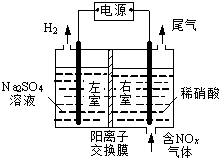 电解法处理含氮氧化物废气,可回收硝酸,具有较高的环境效益和经济效益.实验室模拟电解法吸收NOx的装置如图所示(图中电极均为石墨电极).
电解法处理含氮氧化物废气,可回收硝酸,具有较高的环境效益和经济效益.实验室模拟电解法吸收NOx的装置如图所示(图中电极均为石墨电极).查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
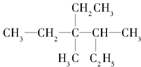 的正确命名为( )
的正确命名为( )| A. | 3-甲基4,4-二乙基戊烷 | B. | 3-甲基3,4-二乙基戊烷 | ||
| C. | 4-甲基2,2-二乙基己烷 | D. | 3,4-二甲基3-乙基己烷 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1mol•L-1NaCl溶液中含有NA个Na+ | |
| B. | 25℃,101kPa,64gSO2中含有的原子数为3NA | |
| C. | 在常温常压下,22.4LCl2含有的分子数为NA | |
| D. | 标准状况下,11.2LCCl4含有的分子数为0.5NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 17 g甲基(-14CH3)所含电子数为10NA | |
| B. | 标准状况下,0.56L丙烷中含有共价键的数目为0.2NA | |
| C. | 在反应KClO3+6HCl=KCl+3Cl2↑+3H2O中,每生成3molCl2转移的电子数为5NA | |
| D. | 0.1mol9038Sr原子中含中子数为3.8NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 任何化学反应都能设计成原电池 | |
| B. | 原电池两极均发生还原反应 | |
| C. | 原电池中的阳离子向负极移动 | |
| D. | 把锌粒放入盛有盐酸的试管中,加入几滴氯化铜溶液,气泡放出速率加快 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com