
 现需配制1.2mol/L NaOH溶液480mL.
现需配制1.2mol/L NaOH溶液480mL.| 50g | 20g | 20g | 10g | 5g |
| ↓↑ |
| n |
| V |
| 50g | 20g | 20g | 10g | 5g |
| ↓↑ | ↓ | ↓↑ | ↓↑ | ↓↑ |


科目:高中化学 来源: 题型:
| A、向NH4Al(SO4)2溶液中滴入Ba(OH)2恰好使SO42-反应完全:NH4++2Ba2++4OH-+Al3++2SO42-=2BaSO4↓+Al(OH)3↓+NH3?H2O | ||||
| B、向海带灰浸出液中加入硫酸、双氧水:2I-+2H++2H2O2=I2+2H2O | ||||
| C、用惰性电极电解MgCl2溶液:2Cl-+2H2O=Cl2↑+H2↑+2OH- | ||||
D、向沸水中逐滴滴入5-6滴饱和FeCl3溶液,继续煮沸至溶液呈红褐色:Fe3++3H2O
|
查看答案和解析>>
科目:高中化学 来源: 题型:
A、14+
| ||||
B、14+
| ||||
C、
| ||||
D、
|
查看答案和解析>>
科目:高中化学 来源: 题型:
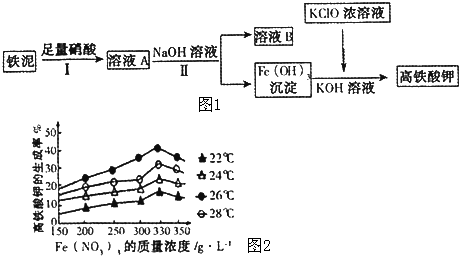
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
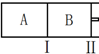 如图所示,A容器充入N2,B容器中充入CO2,隔板I、Ⅱ均可自由移动且保持温度相同,若两容器中所含原子总数相等,则A容器和B容器的容积比为
如图所示,A容器充入N2,B容器中充入CO2,隔板I、Ⅱ均可自由移动且保持温度相同,若两容器中所含原子总数相等,则A容器和B容器的容积比为查看答案和解析>>
科目:高中化学 来源: 题型:
| A、称取硫酸铜晶体16.0g |
| B、称量固体时,天平指针偏左 |
| C、选用的容量瓶内留有少量的蒸馏水 |
| D、定容摇匀后,发现液面低于环形标线,再加水至刻度线 |
查看答案和解析>>
科目:高中化学 来源: 题型:
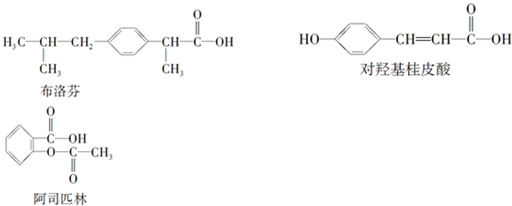
| A、三种有机物都能发生水解反应 |
| B、使用FeCl3溶液和稀硫酸可以鉴别这三种有机物 |
| C、三种有机物苯环上的氢原子若被氯原子取代,其一氯代物都只有2种 |
| D、将等物质的量的三种物质加入氢氧化钠溶液中,对羟基桂皮酸消耗氢氧化钠最多 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com