
| A. | 32g | B. | 50g | C. | 72g | D. | 80g |
分析 如果全部是铜,根据得失电子守恒,则铜的物质的量为:n(Cu)=n(SO2)=$\frac{11.2L}{22.4L/mol}$=0.5mol;如果全部是Cu2O,根据得失电子守恒,则n(Cu2O)=n(SO2)=$\frac{11.2L}{22.4L/mol}$=0.5mol;由此分析解答.
解答 解:如果全部是铜,根据得失电子守恒,则铜的物质的量为:n(Cu)=n(SO2)=$\frac{11.2L}{22.4L/mol}$=0.5mol,质量为32g;如果全部是Cu2O,根据得失电子守恒,则n(Cu2O)=n(SO2)=$\frac{11.2L}{22.4L/mol}$=0.5mol,质量为:144×0.5=72g,所以质量在32g~72g之间,故选B.
点评 本题考查了混合物反应的计算,题目难度中等,明确发生反应的实质为解答关键,注意掌握质量守恒定律、电子守恒在化学计算中的应用,试题培养了学生的分析能力及化学计算能力.


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:选择题
| A | B | C | D | |
实验 | 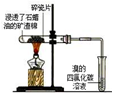 | 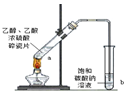 |  |  |
| 现象 | 溴的四氯化碳溶液褪色 | 试管b中出现分层现象 | 量筒内壁出现油状液滴 | 反应过程中钠未熔化成小球 |
| 解释 | 石蜡油分解产物中仅含有乙烯 | 反应生成难溶于饱和碳酸钠溶液的乙酸乙酯 | 甲烷和氯气反应生成了CH2Cl2、CHCl3、CCl4 | 反应吸热 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 具有规则几何外形的固体均为晶体 | |
| B. | 晶体具有自范性,非晶体没有自范性 | |
| C. | 没有固定熔点 | |
| D. | 将玻璃加工成规则的固体即变成晶体 |
查看答案和解析>>
科目:高中化学 来源: 题型:计算题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
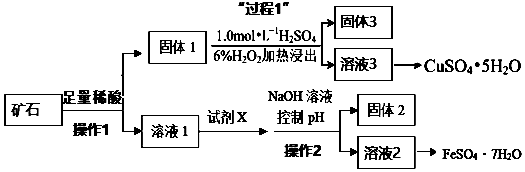
查看答案和解析>>
科目:高中化学 来源: 题型:实验题

查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 8.5 | B. | 17 | C. | 16 | D. | 34 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 相同条件下,2 mol SO2(g)和1 mol O2(g)所具有的能量小于2 mol SO3(g)所具有的能量 | |
| B. | 2 mol SO2(g)和1 mol O2(g)在密闭容器中充分反应,放出热量小于Q kJ | |
| C. | 增大压强或升高温度,该反应过程都能放出更多的热量 | |
| D. | 2 mol SO2(g)和1 mol O2(g)在密闭容器中充分反应,放出热量等于Q kJ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
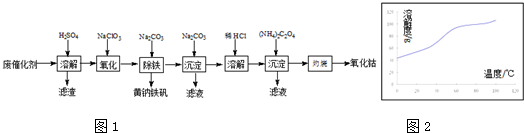
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com