
| A、乙烯和溴单质反应:CH2═CH2+Br2→CH2-CH2Br2 | |||
B、合成聚乙烯塑料:nCH2═CH2→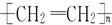 | |||
C、皂化反应: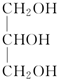 +3H2O +3H2O
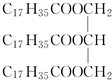 +3C17H35COOH +3C17H35COOH | |||
| D、乙醇与金属钠反应:2CH3CH2OH+2Na→2CH3CH2ONa+H2↑ |
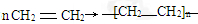 ,故B错误;
,故B错误;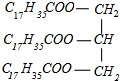 +3NaOH→3C17H35COONa+
+3NaOH→3C17H35COONa+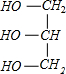 ,故C错误;
,故C错误;

 轻巧夺冠周测月考直通中考系列答案
轻巧夺冠周测月考直通中考系列答案科目:高中化学 来源: 题型:
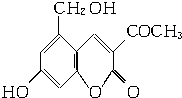 2006年5月,齐齐哈尔第二制药厂生产的假药“亮菌甲素注射液”导致多名患者肾功能衰竭.“亮菌甲素”的结构简式如图,它配以辅料丙二醇溶成针剂用于临床.假药中使用廉价的二甘醇作为辅料,二甘醇为工业溶剂,有很强的毒性.请回答下列问题:
2006年5月,齐齐哈尔第二制药厂生产的假药“亮菌甲素注射液”导致多名患者肾功能衰竭.“亮菌甲素”的结构简式如图,它配以辅料丙二醇溶成针剂用于临床.假药中使用廉价的二甘醇作为辅料,二甘醇为工业溶剂,有很强的毒性.请回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:
 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 2 | ① | ② | ||||||
| 3 | ③ | ④ | ⑤ | ⑥ | ⑦ | ⑧ | ⑨ | |
| 4 | ⑩ | ? | ? |
查看答案和解析>>
科目:高中化学 来源: 题型:
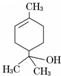
| A、分子式为C10H16O |
| B、能使酸性高锰酸钾溶液褪色 |
| C、分子中含有两种官能团 |
| D、能够与乙酸发生酯化反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、W、X、Y、Z的原子半径大小顺序可能是:W>X>Y>Z |
| B、WY2分子中δ键与π键的数目之比是1:1 |
| C、Y、Z形成的分子空间构型可能是直线形 |
| D、W、Y、Z的电负性大小顺序一定是Z>Y>W |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、18g H2O中含有的质子数为10NA |
| B、在25℃,101kPa时,22.4L氢气中含有NA个氢原子 |
| C、46g NO2和N2O4混合气体中含有原子总数为2NA |
| D、1molNa与足量O2反应,生成Na2O和Na2O2的混合物,钠失去NA个电子 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、将等体积pH=4的盐酸和醋酸稀释到pH=5的溶液,醋酸所加的水量多 |
| B、氯化钠溶液呈中性,醋酸钠溶液呈碱性 |
| C、相同pH的盐酸和醋酸分别跟锌反应时,产生氢气的起始速率相等 |
| D、等体积、相同pH的盐酸和醋酸溶液中分别加入相应的钠盐固体,醋酸pH变大 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、c(OH-)>c(HF)>c(CH3COOH)>c(H+) |
| B、c(OH-)>c(F-)>c(CH3COO-)>c(H+) |
| C、c(F-)+c(CH3COO-)=2c(Na+) |
| D、c(HF)+c(CH3COOH)+c(H+)=c(OH-) |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、用铝锅可长时间盛放酸性食物 |
| B、自来水中通入少量Cl2进行消毒杀菌 |
| C、用小苏打(NaHCO3)发酵面团制作馒头 |
| D、用食醋可除去水壶中的水垢 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com