
 .
. .1molA转化成异丁烷消耗氢气的体积为22.4L(标准状况).
.1molA转化成异丁烷消耗氢气的体积为22.4L(标准状况).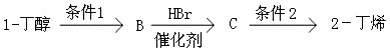
 .
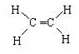
. 分析 (1)乙烯是衡量一个国家石油化工发展水平的重要标志;
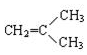
(2)异丁烷的结构简式为CH(CH3)3,A与氢气发生加成反应生成异丁烷,碳链骨架不变,且1:1加成;
(3)由合成流程可知,CH3CH2CH2CH2OH先发生消去反应生成B为CH3CH2CH=CH2,再与HBr发生加成反应生成C为CH3CH2CHBrCH3,最后发生消去反应生成CH3CH=CHCH3,以此来解答.
解答 解:(1)乙烯是衡量一个国家石油化工发展水平的重要标志,乙烯的结构式为 ,故答案为:
,故答案为: ;
;
(2)异丁烷的结构简式为CH(CH3)3,A与氢气发生加成反应生成异丁烷,碳链骨架不变,则A的结构简式为 ,1molA转化成异丁烷消耗氢气的体积为1mol×22.4L/mol=22.4L,
,1molA转化成异丁烷消耗氢气的体积为1mol×22.4L/mol=22.4L,
故答案为: ;22.4;
;22.4;
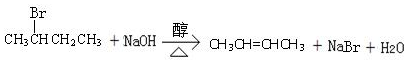
(3)由合成流程可知,CH3CH2CH2CH2OH先发生消去反应生成B为CH3CH2CH=CH2,再与HBr发生加成反应生成C为CH3CH2CHBrCH3,最后发生消去反应生成CH3CH=CHCH3,反应1为醇的消去反应,条件是浓硫酸、加热,C生成2-丁烯的化学方程式为 ,
,
故答案为:浓硫酸、加热; .
.
点评 本题考查有机物的合成,为高频考点,把握官能团的变化、有机反应为解答的关键,侧重分析与应用能力的考查,注意有机物性质的应用,(3)为解答的难点,题目难度不大.


科目:高中化学 来源: 题型:解答题
| 溶解度(S)/g | 溶度积(Ksp) | 摩尔质量(M)/g•mol-1 | |||
| Ca(OH)2 | Ba(OH)2 | CaCO3 | BaCO3 | CaCO3 | BaCO3 |
| 0.16 | 3.89 | 2.9×10-9 | 2.6×10-9 | 100 | 197 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | NH4+、NO3-、Cl-、Na+ | B. | MnO4-、Ca2+、NO3-、Cl- | ||
| C. | HSO3-、HCO3-、NO3-、SO32- | D. | Na+、Ca2+、NO3-、CH3COO- |
查看答案和解析>>
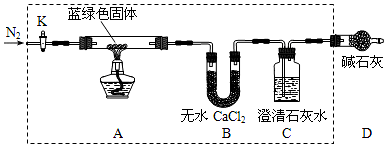
科目:高中化学 来源: 题型:实验题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 托盘天平、烧杯、容量瓶、玻璃棒 | |
| B. | 烧杯、玻璃棒、胶头滴管、量筒 | |
| C. | 烧杯、容量瓶、玻璃棒、胶头滴管 | |
| D. | 烧杯、容量瓶、玻璃棒、胶头滴管、量筒 |
查看答案和解析>>
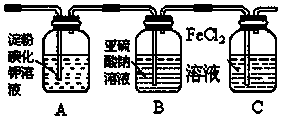
科目:高中化学 来源: 题型:解答题
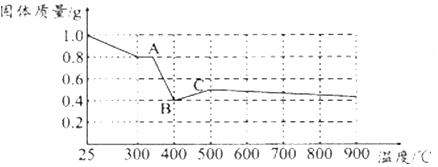
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | WX2分子中所有原子最外层都为8电子结构 | |
| B. | WX2、ZX2是酸性氧化物 | |
| C. | X与Z的氢化物中沸点较高的是Z | |
| D. | WX2中只含有极性键 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Fe 2+、CH 3COOˉ、SO 42ˉ、Na + | B. | Ca 2+、K +、Cl-、HCO 3- | ||
| C. | NH 4+、Al 3+、NO 3-、Cl- | D. | K +、Na +、SO 32-、AlO 2- |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
| 实验目的 | 试剂及方法 |
| 证明某地雨水呈酸性 | A |
| 检验自来水中是否含有Cl- | C |
| 除去FeCl2溶液中的少量FeCl3 | B |
| 除去Fe2O3中的Al2O3 | D |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com