
| W | |||||||
| X | Y | Z |
 .
. 分析 X、Y、Z三种元素位于相同周期且相邻,设X的原子序数为n,则Y、Z的原子序数分别为n+1、n+2,则n+n+1+n+2=21,n=6,则X为C元素,Y为N元素,Z为O元素,由W在周期表中的位置可知为H元素,W与Z可形成原子个数比为1:1的化合物为H2O2,以此解答该题.
解答 解:设X的原子序数为n,则Y、Z的原子序数分别为n+1、n+2,则n+n+1+n+2=21,n=6,
则X为C元素,Y为N元素,Z为O元素,
由W在周期表中的位置可知为H元素,
W与Z可形成原子个数比为1:1的化合物为H2O2,为共价化合物,电子式为 ,
,
故答案为: .
.
点评 本题考查结构性质位置关系应用,为高频考点,侧重于学生的分析能力的考查,难度不大,根据位置判断元素所处的周期是推断关键,注意掌握元素周期表的结构与元素周期律.


 学而优衔接教材南京大学出版社系列答案
学而优衔接教材南京大学出版社系列答案 小学课堂作业系列答案
小学课堂作业系列答案 金博士一点全通系列答案
金博士一点全通系列答案科目:高中化学 来源: 题型:解答题
 、④HCHO,其中碳原子采取sp2杂化的分子有①③④
、④HCHO,其中碳原子采取sp2杂化的分子有①③④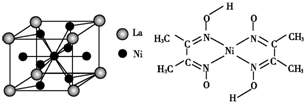
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 实验操作 | 实验现象 | 实验结论 |
| 取适量铁钉与稀硫酸浸泡后的溶液于试管中,依次滴入适量的氯水和几滴KSCN溶液,振荡. | 溶液呈血红色 | 乙同学的观点正确 (填“正确”或“错误”). |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 中和热测定实验中,缓慢地将NaOH溶液倒入测定装置中--测定结果无影响 | |
| B. | 酸碱中和滴定实验中,滴定前无气泡而滴定后有气泡_测定结果偏高 | |
| C. | 测定溶液pH的实验中,用干燥pH试纸测定新制氯水的pH--测定结果无影响 | |
| D. | 现需90mL 1.0mol•L-1NaOH溶液,称取3.6gNaOH固体配制--溶液浓度偏低 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 16O2与18O2互为同位素 | |
| B. | 16O与18O核外电子排布方式相同 | |
| C. | 通过化学变化可以实现16O与18O间的相互转化 | |
| D. | 1.12 L 16O2和1.12 L 18O2均含0.1NA个氧原子 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com