
在前一个分散系中慢慢地滴入后一种分散系所观察到的现象不是先沉淀后变澄清的是
A.氢氧化铁胶体中滴加盐酸 B.偏铝酸钠溶液中加盐酸
C.氯化铝溶液中滴加氢氧化钠溶液 D.氯化铝溶液中滴加氨水
科目:高中化学 来源: 题型:
某同学设计了如下实验测量m g铜银合金样品中铜的质量分数:

下列说法中不正确的是 ( )
A.合金的熔点比其成分金属低,通常比成分金属具有更优良的金属特性
B.铜银都能与稀硝酸反应,收集到的V L气体可能全为NO
C.操作Ⅰ是过滤,操作Ⅱ是洗涤,操作Ⅲ应是烘干
D.根据反应收集到的气体体积可以计算铜和银的质量分数
查看答案和解析>>
科目:高中化学 来源: 题型:
A、B、C、D、E均为易溶于水的化合物,其离子组成如下。(各化合物中离子组成不重复)
| 阳离子 | Na+、Al3+、Ag+、Ba2+、Fe3+ |
| 阴离子 | Cl-、CO |
分别取溶液进行如下实验:
①用pH试纸分别测得B、C溶液均呈碱性,且0.1 mol/L B溶液pH>13;
②D溶液加入铜粉,溶液质量增加;
③在E溶液中加过量B,没有沉淀产生;
④在A溶液中逐滴滴入氨水至过量,先先成白色沉淀,后沉淀溶解。
请回答下列问题:
(1)B的名称:________,E的名称:________。
(2)C水溶液呈碱性的原因(用离子方程式表示):________;0.1 mol/L的C溶液中和0.1 mol/L的NaHCO3溶液中,阴离子的总数:C溶液________NaHCO3溶液。(填“>”、“=”或“<”)
(3)D溶液呈________(填“酸性”、“碱性”或“中性”);若将D溶液加热蒸干,得到的固体应是:________________________。(填化学式)
查看答案和解析>>
科目:高中化学 来源: 题型:
金属钛对人体体液无毒且有惰性,能与肌肉和骨骼生长在一起,有“生物金属”
之称.下列有关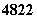 Ti和
Ti和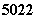 Ti 的说法中正确的是
Ti 的说法中正确的是
A.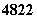 Ti和
Ti和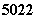 Ti的质量数相同,互称为同位素
Ti的质量数相同,互称为同位素
B.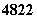 Ti和
Ti和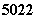 Ti的质子数相同,互称同位素
Ti的质子数相同,互称同位素
C.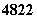 Ti和
Ti和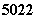 Ti的质子数相同,是同一种核素
Ti的质子数相同,是同一种核素
D.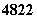 Ti和
Ti和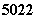 Ti核外电子数相同,中子数不同,不能互称为同位素
Ti核外电子数相同,中子数不同,不能互称为同位素
查看答案和解析>>
科目:高中化学 来源: 题型:
向一定量的K2CO3溶液中缓慢滴加稀盐酸,并不断搅拌。随着盐酸的加入,溶
 液中离子数目也相应地发生变化。如图所示,四条曲线与溶液中的离子的对应关系,完全正确的是
液中离子数目也相应地发生变化。如图所示,四条曲线与溶液中的离子的对应关系,完全正确的是
| a | b | c | d | |
| A | Cl— | K+ | CO32— | HCO3— |
| B | K+ | CO32— | Cl— | HCO3— |
| C | K+ | CO32— | HCO3— | Cl— |
| D | K+ | HCO3— | Cl— | CO32— |
查看答案和解析>>
科目:高中化学 来源: 题型:
物质的量之比为2:5的锌与稀硝酸恰好完全反应,若硝酸被还原的产物为N2O,
反应结束后锌没有剩余,则该反应中被还原的硝酸与未被还原的硝酸的物质的量之比是
A. 1:4 B.1:5 C. 2:3 D.2:5
查看答案和解析>>
科目:高中化学 来源: 题型:
莽草酸是合成治疗禽流感的药物——达菲(Tamiflu)的原料之一。莽草酸是A的一种异构体。A的结构简式如下:
ഠ
(1)A的分子式是 。
(2)A与溴的四氯化碳溶液反应生成物的结构简式是
(3)A与氢氧化钠溶液反应的化学方程式(有机物用结构简式表示)是
(4)17.4克A与足量碳酸氢钠溶液反应,计算生成二氧化碳的体积 (标准状况)。(5)A在浓硫酸作用下加热可得到B(B的结构简式为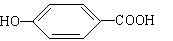 ),其反应类型 。
),其反应类型 。
(6)B的同分异构体中既含有酚羟基又含有酯基的共有 种,写出其中一种同分异构体的结构简式 。
查看答案和解析>>
科目:高中化学 来源: 题型:
强酸和强碱的稀溶液的中和热可表示为:
H+(aq)+OH-(aq)=H2O(1) △H = -57.3kJ/mol
已知:CH3COOH(aq)+NaOH(aq)=CH3COONa(aq)+H2O(1) △H =- Q1kJ/mol
1/2 H2SO4(浓) + NaOH(aq) == 1/2Na2SO4(aq) +H2O(1) △H =- Q2kJ/mol
HNO3(aq)+KOH(aq)=KNO3(aq)+H2O(1) △H =- Q3kJ/mol
上述反应均为溶液中的反应,则Q1、Q2、Q3的绝对值大小的关系为
A.Q1=Q2=Q3 B.Q2>Q1>Q3 C.Q2>Q3>Q1 D.Q2=Q3>Q1
查看答案和解析>>
科目:高中化学 来源: 题型:
下列叙述中正确的是
A.Li是最轻的金属,也是活动性极强的金属,是制造电池的理想物质
B.蔗糖、油脂及它们的水解产物均为非电解质
C.海水提取溴、煤的液化、焰色反应都发生了化学变化
D.钢铁在海水中比在河水中更易被腐蚀,主要原因是海水含氧量高
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com