
£Ø1£©ČōŌŚæÕĘųÖŠ¼ÓČČMgCl2”¤6H2O£¬Éś³ÉµÄŹĒMg(OH)Cl»ņMgO£¬Š“³öĻąÓ¦·“Ó¦µÄ»Æѧ·½³ĢŹ½_________________________________________________”£ÓƵē½ā·ØÖĘČ”½šŹōĆ¾Ź±£¬ŠčŅŖĪŽĖ®ĀČ»ÆĆ¾”£ŌŚøÉŌļµÄHClĘųĮ÷ÖŠ¼ÓČČMgCl2”¤6H2OŹ±£¬ÄܵƵ½ĪŽĖ®MgCl2£¬ĘäŌŅņŹĒ___________________________________”£
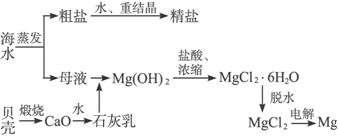
£Ø2£©Mg(OH)2³ĮµķÖŠ»ģÓŠµÄCa(OH)2Ó¦ŌõŃł³żČ„£æŠ“³öŹµŃé²½Öč”£
£Ø3£©ŹµŃéŹŅĄļ½«“ÖŃĪÖĘ³É¾«ŃĪµÄ¹ż³ĢÖŠ£¬ŌŚČܽā”¢¹żĀĖ”¢Õō·¢Čżøö²½ÖčµÄ²Ł×÷ÖŠ¶¼ŅŖÓƵ½²£Į§°ō£¬·Ö±šĖµĆ÷ŌŚÕāČżÖÖĒéæöĻĀŹ¹ÓĆ²£Į§°ōµÄÄæµÄ”£__________________________________
_____________________________________________________________________ӣ
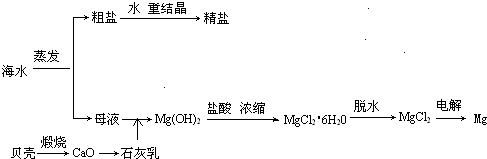
½āĪö£ŗ±¾ĢāŅŌ¹¤ŅµÖĘĆ¾ĪŖ±³¾°£¬Ö÷ŅŖæ¼²éĮĖŹµŃéµÄ»ł±¾²Ł×÷”££Ø1£©ŌŚæÕĘųÖŠ¼ÓČČMgCl2”¤6H2O,MgCl2Ź×ĻČČܽāŌŚĘä½į¾§Ė®ÖŠ£¬²¢·¢ÉśĖ®½ā£ŗMgCl2+2H2O![]() Mg(OH)2+2HCl”üĖę×ÅĖ®·ÖµÄÕō·¢£¬HClŅ»Ķ¬ŅŻ³ö£¬×īŗóĖłµĆ¹ĢĢåĪŖMg(OH)Cl(¼īŹ½ĀČ»ÆĆ¾)»ņMgO”£ÕāŃł£¬·“Ó¦ĪļŗĶÉś³ÉĪļ¶¼ŹĒĆ÷Č·µÄ£ŗ·“Ó¦ĪļĪŖMgCl2”¤6H2O£¬Éś³ÉĪļĪŖMg(OH)Cl»ņMgO”¢HClŗĶH2O£¬Š“³ö·“Ó¦·½³ĢŹ½ÅäĘ½¼“æÉ”£
Mg(OH)2+2HCl”üĖę×ÅĖ®·ÖµÄÕō·¢£¬HClŅ»Ķ¬ŅŻ³ö£¬×īŗóĖłµĆ¹ĢĢåĪŖMg(OH)Cl(¼īŹ½ĀČ»ÆĆ¾)»ņMgO”£ÕāŃł£¬·“Ó¦ĪļŗĶÉś³ÉĪļ¶¼ŹĒĆ÷Č·µÄ£ŗ·“Ó¦ĪļĪŖMgCl2”¤6H2O£¬Éś³ÉĪļĪŖMg(OH)Cl»ņMgO”¢HClŗĶH2O£¬Š“³ö·“Ó¦·½³ĢŹ½ÅäĘ½¼“æÉ”£
ŌŚøÉŌļµÄHClĘųĮ÷ÖŠ¼ÓČČMgCl2”¤6H2O£¬MgCl2µÄĖ®½āŹÜµ½ŅÖÖĘ£¬Ķ¬Ź±MgCl2ČÜŅŗÖŠµÄĖ®Ęū±»HCl(g)“ų×ߣ¬×īŗóÖ»µĆĪŽĖ®MgCl2”£
£Ø2£©Mg(OH)2ÖŠŗ¬ÓŠCa(OH)2£¬æɽ«Ca(OH)2Čܽā¶ų³żČ„£¬ÓÉÓŚCa(OH)2Ī¢ČÜÓŚĖ®£¬Ņņ“ĖŠė½«Ęä×Ŗ»ÆĪŖŅ×ČÜÓŚĖ®µÄĪļÖŹ”£¼ųÓŚOH-²»ŹĒŌÓÖŹ£¬Ņņ“ĖÓĆMgCl2ČÜŅŗ½ĻĪŖŗĻŹŹ£ŗ
Ca(OH)2+MgCl2====CaCl2+Mg(OH)2”żÕāŃł£¬¹żĀĖµĆµ½Mg(OH)2£¬»¹ŠčĻ“µÓŅŌ³żČ„Ęä±ķĆęø½×ŵÄCaCl2”£
“š°ø£ŗ£Ø1£©MgCl2”¤6H2O![]() Mg(OH)Cl+HCl”ü+5H2O
Mg(OH)Cl+HClӟ+5H2O
MgCl2”¤6H2O![]() MgO+2HCl+5H2O”²»ņMg(OH)Cl
MgO+2HCl+5H2O”²»ņMg(OH)Cl![]() MgO+HCl”ü”³
MgO+HCl”ü”³
ŌŚøÉŌļµÄHClĘųĮ÷ÖŠ£¬ŅÖÖĘĮĖMgCl2Ė®½ā£¬ĒŅ“ų×ßMgCl2”¤6H2OŹÜČČ²śÉśµÄĖ®Ęū£¬¹ŹÄܵƵ½ĪŽĖ®MgCl2
£Ø2£©¼ÓČėMgCl2ČÜŅŗ£¬³ä·Ö½Į°č£¬¹żĀĖ£¬³ĮµķÓĆĖ®Ļ“µÓ”£
£Ø3£©a£ŗ½Į°č£¬¼ÓĖŁČܽā
b£ŗŹ¹“żĀĖŅŗĢåŃŲ²£Į§°ōĮ÷ČėĀ©¶·£¬·ĄÖ¹ĶāČ÷
c£ŗ½Į°č£¬·ĄÖ¹Ņņ¾Ö²æ¹żČČŅŗµĪ»ņ¾§Ģå·É½¦


 µ¼Ń§½Ģ³ĢøßÖŠŠĀæĪ±źĻµĮŠ“š°ø
µ¼Ń§½Ģ³ĢøßÖŠŠĀæĪ±źĻµĮŠ“š°ø
| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ

| ||
| ||
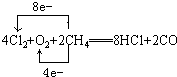
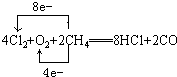
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ²»Ļź ĢāŠĶ£ŗĪŹ“šĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ×ØĻīĢā ĢāŠĶ£ŗĢīæÕĢā

²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ

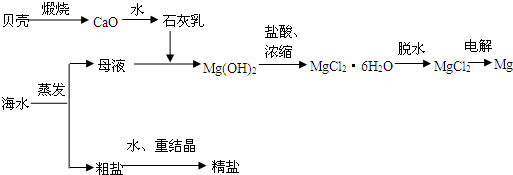
(1)ŌŚæÕĘųÖŠ¼ÓČČMgCl2”¤6H2O£¬¼ŁÉčÄÜÉś³ÉMgOŗĶHCl£¬Š“³öĻąÓ¦µÄ·“Ó¦µÄ»Æѧ·½³ĢŹ½£ŗ____________________________________________________________________”£
ÖĘČ”½šŹōĆ¾Ź±£¬æÉŅŌÓƵē½āMgCl2µÄ·½·Ø£¬Š“³öĻąÓ¦µÄ·“Ó¦µÄ»Æѧ·½³ĢŹ½£ŗ________________________________________”£
(2)µē½āĪŽĖ®ĀČ»ÆĆ¾²śĪļÖ®Ņ»µÄCl2æÉÓėæÕĘų”¢¼×ĶéĘš·“Ó¦(²śĪļĪŖHCl”¢CO)£¬ŌŁÖʵĆŃĪĖįŃ»·Ź¹ÓĆ£¬Š“³öøĆ·“Ó¦µÄ»Æѧ·½³ĢŹ½²¢±ź³öµē×Ó×ŖŅʵķ½ĻņŗĶŹżÄæ£ŗ
____________________________________________________________________ӣ
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com