(2010?朝阳区模拟)根据废水中所含有害物质的不同,工业上有多种废水的处理方法.
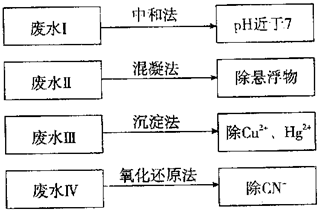
(1)①废水I若采用CO
2处理,离子方程式是
OH-+CO2=HCO3-
OH-+CO2=HCO3-
.
②废水Ⅱ常用明矾处理.实践中发现废水中的c(HCO
-3)越大,净水效果越好,这是因为
HCO3-会促进Al3+的水解,生成更多的Al(OH)3,净水效果增强
HCO3-会促进Al3+的水解,生成更多的Al(OH)3,净水效果增强
.
③废水Ⅲ中的汞元素存在如下转化(在空格上填相应的化学式):Hg
2++
CH4
CH4
═CH
3Hg
++H
+我国规定,Hg
2+的排放标准不能超过0.05mg/L.若某工厂排放的废水1L中含Hg
2+3×10
-7mol,是否达到了排放标准
否
否
(填“是”或“否”).
④废水Ⅳ常用Cl
2氧化CN
-成CO
2和N
2,若参加反应的Cl
2与CN
-的物质的量之比为5:2,则该反应的离子方程式为
5Cl2+2CN-+4H2O=10Cl-+2CO2+N2+8H+
5Cl2+2CN-+4H2O=10Cl-+2CO2+N2+8H+
.
(2)化学需氧量(COD)可量度水体受有机物污染的程度,它是指在一定条件下,用强氧化剂处理水样时所消耗的氧化刹的量,换算成氧的含量(以mg/L计).某研究性学习小组测定某水样的化学需氧量(COD),过程如下:
Ⅰ.取V
1 mL水样于锥形瓶,加入10.00mL 0.2500mol/L K
2Cr
2O
7溶液.
Ⅱ.加碎瓷片少许,然后慢慢加入硫酸酸化,混合均匀,加热.
Ⅲ.反应完毕后,冷却,加指示剂,用c mol/L的硫酸亚铁铵[(NH
4)
2Fe(SO
4)
2]溶液 滴定.终点时消耗硫酸亚铁铵溶液V
2 mL.
①I中,量取K
2Cr
20
7,溶液的仪器是
酸式滴定管(或移液管)
酸式滴定管(或移液管)
.
②Ⅱ中,碎瓷片的作用是
防止暴沸
防止暴沸
.
③Ⅲ中,发生的反应为:Cr
2O
72-+6Fe
2++14H
+═2Cr
3++6Fe
3+7H
2O由此可知,该水样的化学需氧量COD=
(用含c、V
1、V
2的表达式表示).

 每日10分钟口算心算速算天天练系列答案
每日10分钟口算心算速算天天练系列答案