
【题目】已知木炭在一定条件下与浓硝酸反应生成两种+4价的氧化物,为了探究一氧化氮(NO)能否与过氧化钠反应,以及反应后的产物中是否有亚硝酸钠(NaNO2),某小组同学设计了如图所示装置(夹持仪器和连接用的胶管已经省略)。
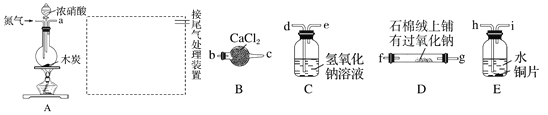
(1)为了完成该实验,虚线框内还需要连接B~E四套装置,按气流方向连接的顺序为:
a→( )( )→( )( )→( )( )→ ( )( )(填仪器接口的字母编号)。连接好仪器,检查气密性,装入药品后,要通入一段时间的氮气,再滴加浓硝酸,点燃酒精灯,通入氮气的主要目的是 。
(2)装置E中观察到的主要实验现象有 。
(3)装置C的作用是 。
(4)某同学经查阅资料后发现亚硝酸是弱酸,性质不稳定,室温下易分解生成一氧化氮。装置D中充分反应后,设计实验证明D中是否有亚硝酸钠生成: 。(写出检验步骤及现象)。
(5)亚硝酸钠在酸性条件下可将I-氧化为I2,同时生成NO,该反应常用于亚硝酸钠含量的测定,请写出该反应的离子方程式: 。
【答案】(1)hi→de→bc→fg(或gf)排除装置中的空气,防止NO被空气中氧气氧化为NO2;
(2)溶液由无色变成蓝色,有无色气体逸出
(3)吸收CO2,除去NO中的NO2
(4)取少量D中的固体于试管中,加入稀硫酸,若溶液中有气泡产生且在试管液面上方变成红棕色气体,则D中有亚硝酸钠生成。
(5)2NO2-+2I-+4H+=2NO↑+I2+2H2O
【解析】木炭与浓硝酸反应在加热条件下生成NO2和CO2,装置E是将NO2溶于水转化成NO和HNO3,稀硝酸和铜反应又生成NO;装置C的作用是吸收CO2,除去NO中的NO2;装置B的作用起干燥作用;亚硝酸不稳定,易分解生成NO,所以检验亚硝酸钠,是将其变成HNO2,检验其产物NO就行了;


 优百分课时互动系列答案
优百分课时互动系列答案 开心蛙状元作业系列答案
开心蛙状元作业系列答案科目:高中化学 来源: 题型:
【题目】电化学原理在防止金属腐蚀、能量转换、物质合成等方面应用广泛。
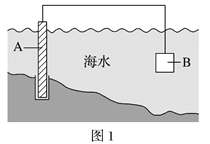
(1)图1中,为了减缓海水对钢闸门A的腐蚀,材料B可以选择__________(填字母序号)
a.碳棒 b.锌板 c.铜板
用电化学原理解释材料B需定期拆换的原因_______________。
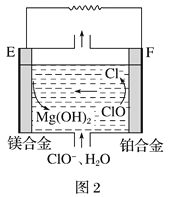
(2)镁燃料电池在可移动电子设备电源和备用电源等方面应用前景广阔。图2为“镁—次氯酸盐”燃料电池原理示意图,电极为镁合金和铂合金。
①E为该燃料电池的_____________极(填“正”或“负”)。F电极上的电极反应式为_____________。
②镁燃料电池负极容易发生自腐蚀产生氢气,使负极利用率降低,用化学用语解释其原因____________。
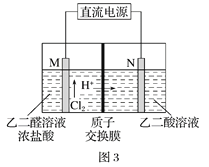
(3)乙醛酸(HOOC-CHO)是有机合成的重要中间体。工业上用“双极室成对电解法”生产乙醛酸,原理如图3所示,该装置中阴、阳两极为惰性电极,两级室均可产生乙醛酸,其中乙二醛与M电极的产物反应生成乙醛酸。
①N电极上的电极反应式为______________。
②若有2molH+通过质子交换膜,并完全参与了反应,则该装置中生成的乙醛酸为________________mol。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某课外活动小组利用下图装置进行碱式碳酸钴[Cox(OH)y(CO3)z]的化学组成测定的探究实验,图中铁架台等装置已略去,粗黑线表示乳胶管。
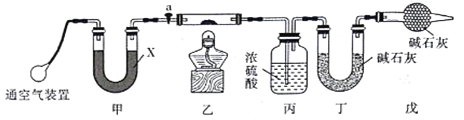
已知碱式碳酸钴受热时按右式分解:碱式碳酸钴![]() 钴的氧化物+CO2↑+H2O↑。
钴的氧化物+CO2↑+H2O↑。
回答下列问题:
(l)按如图所示装置组装好仪器,在装药品前,应先进行的操作是_______。
(2)称取3.65g样品置于硬质玻璃管内;打开活塞a,缓缓通入空气数分钟,关闭活塞a;加热硬质玻璃管,当丙装置中不再有气泡产生时,停止加热;又打开活塞a,再缓缓通入空气数分钟。两次通入空气的目的不同,第一次的目的是将装置中含二氧化碳和水蒸气的空气排尽,第二次的目的是______。
(3)通过正确实验测得丙、丁装置增重分别为0.36g、0.88g,则该碱式碳酸钴的化学式为______。
(4)甲装置中X试剂是______(填标号)。
a.浓硫酸 b.水氯化钙 c.五氧化二磷粉末 d.碱石灰
(5)若去掉戊装置,会使x的值______(填“偏大”“偏小”或“不变”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】关于碱金属单质的性质叙述错误的是( )
A. 都能够在空气中剧烈燃烧
B. 都能够与水反应生成碱和H2
C. 都可以保存在煤油中
D. 都是密度比较小、熔点比较低的金属
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】向20mL0.5mol L-1的醋酸溶液中逐滴加入等物质的量浓度的烧碱溶液,测定混合溶液的温度变化如图所示。下列关于混合溶液的相关说法中错误的是
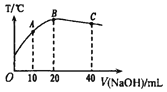
A. 由水电离出的c(H+):C点>B点
B. 醋酸的电离平衡常数:B点> A点
C. 从A点到B点,混合溶液中可能存在:c( CH3COO-) = c(Na+)
D. C 点混合溶液中一定存在:c(Na+) =2c(CH3COO-) +2c(CH3COOH)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A、B、C、D均为中学化学中常见的单质或化合物,它们之间的关系如图a所示(部分产物已略去)。
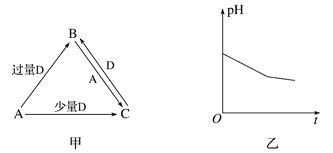
(1)若A为非金属单质,D是空气的主要成分之一,请写出B的电子式______________。
(2)若A为金属单质,D是某强酸的稀溶液,则反应C+D→B的离子方程式为_____________________。
(3)若A为强碱,D为气态氧化物。B的水溶液露置于空气中一段时间,其pH变化如图b所示,则其pH变化的原因是____________(用离子方程式表示)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是
A. 碘酒能使蛋白质发生变性 B. 化工合成的香精均可用作食品添加剂
C. 司母戊鼎的主要成分为铁 D. 铵态氮肥与草木灰混合使用效果更好
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某研究小组以化合物1为原料,按下列路线制备聚合物8。
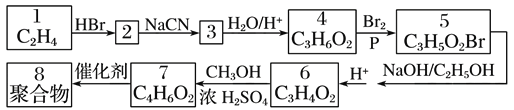
已知:R—X![]() R—CN
R—CN![]() R—COOH
R—COOH
R—CH2COOH![]()
![]()
请回答:
(1)以下四个化合物中,含有羧基的是
A.化合物3 B.化合物4 C.化合物6 D.化合物7
(2)化合物4→8的合成路线中,未涉及的反应类型是
A.取代反应 B.消去反应 C.加聚反应 D.还原反应
(3)下列四个化合物中,与化合物4互为同系物的是
A.CH3COOC2H5B.C6H5COOH
C.CH3CH2CH2COOH D.CH3COOH
(4)化合物4的属于酯类的所有同分异构体的结构简式 。
(5)化合物7→8的化学方程式 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com