
| 实验 序号 | 浓度 时间 温度 | 0 | 10 | 20 | 30 | 40 | 50 | 60 |
| 1 | 800 | 1.0 | 0.80 | 0.67 | 0.57 | 0.50 | 0.50 | 0.50 |
| 2 | 800 | c2 | 0.60 | 0.50 | 0.50 | 0.50 | 0.50 | 0.50 |
| 3 | 800 | c3 | 0.92 | 0.75 | 0.63 | 0.60 | 0.60 | 0.60 |
| 4 | 820 | 1.0 | 0.40 | 0.25 | 0.20 | 0.20 | 0.20 | 0.20 |
分析 (1)根据平均化学反应速率公式:v=$\frac{△c}{△t}$计算;
(2)根据实验1、2数据以及平衡时的浓度判断;
(3)根据浓度对化学反应速率的影响分析;
(4)比较实验4和实验1可知平衡时实验4反应物A的浓度小,由实验1到实验4升高温度.
解答 解:(1)实验①前10min内A的平均反应速率为v=$\frac{△c}{△t}$=$\frac{0.80mol/L-0.67mol/L}{10min}$=0.013mol/(L•min),
故答案为:0.013;
(2)根据实验1、2数据分析,温度相同,达平衡后A的物质的量浓度相同,且B、D起始浓度为0,所以两组实验中A的起始浓度相同为1.0mol•L-1 ,
故答案为:1.0;
(3)实验1、3比较,温度相同,10min-20min时,实验3的浓度减少量都大于实验1的,所以实验3的反应速率大于实验1的,即v3>v1,
故答案为:>;
(4)比较实验4和实验1可知平衡时实验4反应物A的浓度小,由实验1到实验4升高温度,平衡右移,加热平衡向吸热反应方向移动,
故答案为:吸热; 温度升高时,平衡向右移动.
点评 本题考查化学反应速率的影响因素,为高频考点,侧重考查学生的分析能力和计算能力,注意把握化学反应速率的计算及控制变量法应用,题目难度中等.


科目:高中化学 来源: 题型:填空题
 ②CH3CH2CH2CH2OH③
②CH3CH2CH2CH2OH③ ④
④
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 所有的有机物都可以燃烧 | |
| B. | 一定条件下,甲烷、苯、乙酸、乙醉、油脂、淀粉都可以发生取代反应 | |
| C. | 糖类、油脂、蛋白质都厲于高分子化合物 | |
| D. | 石油的分馏、裂化、裂解和煤的干馏都厲于化学变化 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题

| A. | CH3CH2COOCH3 | B. | CH3CH2CH2COOH | C. | HCOOCH2CH2CH3 | D. | HCOOCH(CH3)2 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
 在实验室可以用如图所示的装置制取乙酸乙酯,请回答下列问题.
在实验室可以用如图所示的装置制取乙酸乙酯,请回答下列问题.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | a<b | B. | a=b | C. | a>b | D. | 无法确定 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1molNa2O2固体中含离子总数为4 NA | |
| B. | 分子数为NA的CO、C2H4混合气体体积约为22.4L,质量为28g | |
| C. | 28g由C2H4和C3H6组成的混合物中含有氢原子的数目为4NA | |
| D. | 常温下,1mol Fe与过量浓HNO3反应,转移电子的数目为3 NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
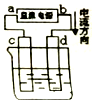
| A. | b为阳极、a为阴极 | |
| B. | 通电一段时间后,d极附近观察到黄绿色气体 | |
| C. | 阳极上发生的反应:Cu2++2e-═Cu | |
| D. | 若电路中转移0.2mole-,则d极增重6.4g |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com