
”¾ĢāÄæ”泤Ź½ÖÜĘŚ±ķ¹²ÓŠ18øöׯĮŠ£¬“Ó×óµ½ÓŅÅÅĪŖ1”«18ĮŠ£¬¼“¼ī½šŹōĪŖµŚ1ĮŠ£¬Ļ”ÓŠĘųĢåŌŖĖŲĪŖµŚ18ĮŠ£®°“ÕāÖÖ¹ę¶Ø£¬ĻĀĮŠĖµ·ØÕżČ·µÄŹĒ£Ø £©
A.µŚ14ĮŠŌŖĖŲÖŠĪ“³É¶Ōµē×ÓŹżŹĒĶ¬ÖÜĘŚŌŖĖŲÖŠ×ī¶ąµÄ
B.Ö»ÓŠµŚ2ĮŠµÄŌŖĖŲŌ×Ó×īĶā²ćµē×ÓÅŲ¼ĪŖns2
C.µŚĖÄÖÜĘŚµŚ8ĮŠŌŖĖŲŹĒĢśŌŖĖŲ
D.µŚ15ĮŠŌŖĖŲŌ×ӵļŪµē×ÓÅŲ¼ĪŖns2np5

| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æµ³µÄŹ®¾Å“ó±ØøęÖø³ö:ŅŖ³ÖŠųŹµŹ©“óĘųĪŪČ¾·ĄÖĪŠŠ¶Æ£¬“ņÓ®Ą¶Ģģ±£ĪĄÕ½”£µ±Ē°æÕĘųÖŹĮæ¼ģ²āµÄÖ÷ŅŖĻīÄæ³żĮĖPM2.5Ķā£¬»¹ÓŠCO”¢SO2”¢µŖŃõ»ÆĪļ(NOŗĶNO2)”¢O3µČĘųĢ唣
(1)Ęū³µĪ²ĘųÖŠŗ¬ÓŠNOŗĶCOĘųĢ壬æÉĄūÓĆ“ß»Æ¼Į¶ŌCO”¢NO½ųŠŠ“ß»Æ×Ŗ»Æ·“Ó¦:
2CO(g)+2NO(g) ![]() N2(g)+2CO2(g) ”÷H
N2(g)+2CO2(g) ”÷H
¢ŁŅŃÖŖĻĀĮŠČČ»Æѧ·½³ĢŹ½:
N2(g)+O2(g)=2NO(g) ”÷H1=+180.5kJ/mol
2C(s)+O2(g)=2CO(g) ”÷H2=-2210kJ/mol
C(s)+O2(g)=CO2(g) ”÷H3=-393.5kJ/mol
Ōņ”÷H=_________”£
¢ŚŌŚŅ»¶ØĪĀ¶ČĻĀ,½«2.0molNO”¢2.4molCOĘųĢåĶØČėµ½¹Ģ¶ØČŻ»żĪŖ2LµÄĆܱÕČŻĘ÷ÖŠ£¬·“Ó¦¹ż³ĢÖŠ²æ·ÖĪļÖŹµÄÅØ¶Č±ä»ÆČēĻĀĶ¼ĖłŹ¾”£ŌŚ0~15min,ŅŌN2±ķŹ¾µÄøĆ·“Ó¦µÄĘ½¾łĖŁ¶Čv(N2)=________”£Čō±£³Ö·“Ó¦ĢåĻµĪĀ¶Č²»±ä£¬20minŹ±ŌŁČŻĘ÷ÖŠ³äČėNO”¢N2ø÷0.4mol£¬»ÆŃ§Ę½ŗā½«_____ŅʶÆ(Ģī”°Ļņ×ó”±”°ĻņÓŅ”±»ņ”°²»”±)”£

(2)ŌŚĻąĶ¬ĪĀ¶ČĻĀ£¬Į½øöĢå»ż¾łĪŖ1LµÄŗćČŻĆܱÕČŻĘ÷ÖŠ£¬·¢ÉśCO”¢NO“ß»Æ×Ŗ»Æ·“Ó¦£¬ÓŠ¹ŲĪļÖŹµÄĮæČēĻĀ±ķ:
ČŻĘ÷±ąŗÅ | ĘšŹ¼ĪļÖŹµÄĮæ/mol | Ę½ŗāĪļÖŹµÄĮæ/mol | |||
NO | CO | N2 | CO2 | CO2 | |
I | 0.2 | 0.2 | 0 | 0 | a |
II | 0.3 | 0.3 | b | 0.1 | 0.2 |
¢ŁČŻĘ÷IÖŠĘ½ŗāŗóĘųĢåµÄŃ¹ĒæĪŖæŖŹ¼Ź±µÄ0.875±¶£¬Ōņa=________”£
¢ŚČŻĘ÷IIĘ½ŗāŹ±µÄĘųĢåŃ¹ĒæĪŖp£¬ÓĆĘ½ŗā·ÖŃ¹“śĢęĘ½ŗāÅØ¶Č±ķŹ¾µÄĘ½ŗā³£ŹżKĪŖ________”£
(3)Ęū³µŹ¹ÓĆŅŅ“¼ĘūÓĶ²¢²»ÄÜĘĘÉŁNOxµÄÅÅ·Å”£Ä³ŃŠ¾æŠ”×éŌŚŹµŃéŹŅŅŌÄĶøßĪĀŹŌ¼ĮAg-ZSW-5¶ŌCO”¢NO“ß»Æ×Ŗ»Æ½ųŠŠŃŠ¾æ”£²āµĆNO×Ŗ»ÆĪŖN2µÄ×Ŗ»ÆĀŹĖęĪĀ¶ČCO»ģ“ęĮæµÄ±ä»ÆĒéæöČēĶ¼ĖłŹ¾”£

¢ŁŌŚn(NO)/n(CO)=1Ģõ¼žĻĀ£¬×ī¼ŃĪĀ¶ČÓ¦æŲÖĘŌŚ_______×óÓŅ”£
¢ŚČō²»Ź¹ÓĆCO£¬ĪĀ¶Č³¬¹ż775K£¬·¢ĻÖNOµÄ·Ö½āĀŹ½µµĶ£¬ĘäæÉÄܵÄŌŅņĪŖ________”£
¢Ū¼ÓČėCOŗóNO×Ŗ»ÆĪŖN2µÄ×Ŗ»ÆĀŹŌö“óµÄŌŅņŹĒ_______ (ÓĆĘ½ŗāŅĘ¶ÆµÄŌĄķ½āŹĶ)”£
(4)ŅŌNO2”¢O2”¢ČŪČŚNaNO3×é³ÉµÄČ¼ĮĻµē³Ų×°ÖĆČēÓŅĶ¼ĖłŹ¾£¬ŌŚŹ¹ÓĆ¹ż³ĢÖŠŹÆÄ«Iµē¼«·“Ӧɜ³ÉŅ»ÖÖŃõ»ÆĪļY£¬ŌņøƵē¼«·“Ó¦Ź½ĪŖ_______”£

²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æŌŚĆܱÕĘųø×ÖŠÓĆŅ»²»Ā©ĘųµÄæÉ×ŌÓÉŅĘ¶ÆµÄ»īČūøōæŖ(ČēĻĀĶ¼)£¬ÓŅ±ß³äÓŠH2ŗĶO2£¬×ó±ß³äÓŠN2£¬ŌŚ20”ꏱ½«ÓŅ±ßµÄ»ģŗĻĘųĢåµćČ¼£¬ĄäČ“µ½ŌĪĀ¶Č”£Čō»īČūŌĄ“¾ąĄėĘųø××ó¶ĖµÄ¾ąĄėĪŖ×ܳ¤µÄ1/4£¬·“Ó¦ŗó»īČū¾²Ö¹ÓŚĘųø×ÖŠµć(Ė®µÄĢå»żŗöĀŌ²»¼Ę)£¬ŌņŌĄ“H2ŗĶO2µÄĢå»ż±ČæÉÄÜĪŖ( )
![]()
A. 2:1 B. 7:2 C. 5:4 D. 8:1
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æ2002ÄźÅµ±“¶ū»Æѧ½±»ńµĆÕߵűĻ×Ö®Ņ»ŹĒ·¢Ć÷ĮĖ¶ŌÓŠ»śĪļ·Ö×Ó½ųŠŠ½į¹¹·ÖĪöµÄÖŹĘ×·Ø”£Ęä·½·ØŹĒČĆ¼«ÉŁĮæµÄ£Ø10£9g£©»ÆŗĻĪļĶعżÖŹĘ×ŅĒµÄĄė×Ó»ÆŹŅŹ¹ŃłĘ··Ö×Ó“óĮæĄė×ӻƣ¬ÉŁĮæ·Ö×ÓĖéĮŃ³ÉøüŠ”µÄĄė×Ó”£ČēC2H6Ąė×Ó»ÆŗóæɵƵ½C2H6£«”¢C2H5£«”¢C2H4£«””£¬Č»ŗó²ā¶ØĘäÖŹŗɱȔ£Ä³ÓŠ»śĪļѳʷµÄÖŹŗɱČČēĻĀĶ¼ĖłŹ¾£Ø¼ŁÉčĄė×Ó¾ł“ųŅ»øöµ„Ī»ÕżµēŗÉ£¬ŠÅŗÅĒæ¶ČÓėøĆĄė×ӵĶąÉŁÓŠ¹Ų£©£¬ŌņøĆÓŠ»śĪļæÉÄÜŹĒ£Ø £©
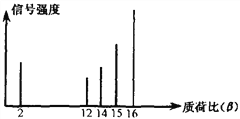

A. ¼×“¼ B. ±ūĶé C. ¼×Ķé D. ŅŅĻ©
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æÖŠ³ÉŅ©Į¬»ØĒåĪĮ½ŗÄŅŌŚ¶Ōæ¹ H1N1²”¶¾ÖŠ·¢»ÓÖŲ“ó×÷ÓĆ£¬ĘäÓŠŠ§³É·ÖĀĢŌĖįµÄ½į¹¹¼ņŹ½ČēĶ¼£¬ĻĀĮŠÓŠ¹ŲĖµ·Ø“ķĪóµÄŹĒ
A. ĀĢŌĖįŹōÓŚ·¼Ļć×å»ÆŗĻĪļ
B. ·Ö×ÓÖŠÖĮÉŁÓŠ 7 øöĢ¼Ō×Ó¹²Ćę
C. 1mol ĀĢŌĖį×ī¶ąæÉĻūŗÄ 5mol NaOH
D. ÓėĀĢŌĖį±½»·ÉĻČ”“ś»łÖÖĄą¼°øöŹż¾łĻąĶ¬µÄÓŠ»śĪļÓŠ5 ÖÖ
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æČēĶ¼ŹĒŹµŃéŹŅ½ųŠŠ¶žŃõ»ÆĮņÖʱøÓėŠŌÖŹŹµŃéµÄ×éŗĻ×°ÖĆ£¬²æ·Ö¹Ģ¶Ø×°ÖĆĪ“»³ö”£ĻĀĮŠÓŠ¹ŲĖµ·ØÕżČ·µÄŹĒ

A. ¹Ų±Õ K2£¬“ņæŖ K1£¬µĪ¼ÓĮņĖį£¬Ōņ×°ÖĆ B ÖŠĆæĻūŗÄ 1molNa2O2£¬×ŖŅʵē×ÓŹżĪŖNA
B. ¹Ų±Õ K1£¬“ņæŖ K2£¬ŹŌ¼Į X ŹĒĖįŠŌ KMnO4 »ņ FeCl3 ČÜŅŗ£¬¾łæÉÖ¤Ć÷ SO2 ÓŠ»¹ŌŠŌ
C. ĪŖ·ĄÖ¹»·¾³ĪŪČ¾£¬×°ÖĆCŗĶEÖŠµÄŹŌ¼Į¾łČ”ÓƱ„ŗĶµÄŹÆ»ŅĖ®
D. ŹµŃé¹ż³ĢÖŠĢåĻÖĮĖĮņĖįµÄĖįŠŌ”¢ĪüĖ®ŠŌ”¢Äѻӷ¢ŠŌ”¢ĒæŃõ»ÆŠŌ
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æ¶ŌA+3B=2C+2DĄ“Ėµ£¬ĻĀĮŠĖÄÖÖ²»Ķ¬ĒéæöĻĀµÄ·“Ó¦ĖŁĀŹ×īæģµÄŹĒ
A. ¦Ō£ØA£©=0.25 mol/£ØL”¤min£© B. ¦Ō£ØB£©=0.6 mol/£ØL”¤min£©
C. ¦Ō£ØC£©=0.5 mol/£ØL”¤min£© D. ¦Ō£ØD£©=0.6 mol/£ØL”¤min£©
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æµŚĖÄÖÜĘŚ¹ż¶ÉŌŖĖŲČēĢś”¢ĆĢ”¢Ķ”¢ŠæµČŌŚĢ«ŃōÄܵē³Ų”¢“ÅŠŌ²ÄĮĻµČæĘ¼¼·½ĆęÓŠ¹ć·ŗµÄÓ¦ÓĆ£¬»Ų“šĻĀĮŠĪŹĢā£ŗ
£Ø1£©ŌŚĻÖ“ś»Æѧ֊£¬³£ĄūÓĆ______ÉĻµÄĢŲÕ÷Ę×Ļߥ“¼ų¶ØŌŖĖŲ£¬³ĘĪŖ¹āĘ×·ÖĪö”£
£Ø2£©Š“³ö Cu2+µÄĶāĪ§µē×ÓÅŲ¼Ź½__________£»±Č½ĻĢśÓėĆĢµÄµŚČżµēĄėÄÜ(I3)£ŗĢś____ĆĢ(Ģī”°£¾”±”¢ ”°£½”±»ņ”°£¼”±)£¬ŌŅņŹĒ________________”£
£Ø3£©ŅŃÖŖ [Zn(CN)4]2-Óė¼×Č©ŌŚĖ®ČÜŅŗÖŠ·¢Éś·“Ó¦æÉÉś³ÉŅ»ÖÖŠĀĪļÖŹ HOCH2CN£¬ŹŌÅŠ¶ĻŠĀĪļÖŹÖŠĢ¼Ō×ÓµÄŌӻƷ½Ź½___________£»1mol[Zn(CN)4]2-ÖŠµÄ ¦Ņ ¼üŹżĪŖ__________”£
£Ø4£©ČēĶ¼ŹĒ¾§Ģå Fe3O4 µÄ¾§°ū£¬øĆ¾§ĢåŹĒŅ»ÖÖ“ÅŠŌ²ÄĮĻ£¬ Äܵ¼µē”£
¢Ł¾§°ūÖŠ¶ž¼ŪĢśĄė×Ó“¦ÓŚŃõĄė×ÓĪ§³ÉµÄ______(ĢīæÕ¼ä½į¹¹)æÕĻ¶”£
¢Ś¾§°ūÖŠŃõĄė×ӵĶѻż·½Ź½Óėij½šŹō¾§ĢåŌ×Ӷѻż·½Ź½ĻąĶ¬£¬øƶѻż·½Ź½Ćū³ĘĪŖ________”£
¢Ū½āŹĶ Fe3O4 ¾§ĢåÄܵ¼µēµÄŌŅņ_________________£»Čō¾§°ūµÄĢå¶Ō½ĒĻß³¤ĪŖ a nm£¬Ōņ Fe3O4 ¾§ĢåµÄĆܶČĪŖ________g”¤cm£3(°¢·ü¼ÓµĀĀŽ³£ŹżÓĆ NA ±ķŹ¾)”£

²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æ±ź×¼×“æöĻĀ£¬32gCH4ĖłÕ¼Ģå»żŌ¼ĪŖ£Ø £©
A. 44.8L B. 22.4L C. 11.2L D. 5.6L
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com