
已知X、Y、Z、W、N是短周期元素中的四种元素,它们的原子序数依次增大.X元素的原子形成的离子就是一个质子,Z、W在元素周期表中处于相邻的位置,它们的单质在常温下均为无色气体,Y原子的最外层电子数是内层电子数的2倍,工业上常用电解w与N的化合物来制备N单质。
(1)请写出Z在元素周期表中的位置________ 。化合物甲由元素X与Z组成,1mol甲含18mol电子,请写出甲的电子式: ;
(2)元素N的一种常见的可溶性盐溶液呈碱性,其原因是(用离子方程式表示): ;
(3)由X、Y、Z、W四种元素中的三种组成的一种强酸,该强酸的稀溶液能与铜反应,其离子方程式为 。
(4)已知离子化合物乙由X、Y、Z、W四种元素组成,乙既能与盐酸反应,又能与NaOH溶液反应,1mol 乙能与过量NaOH浓溶液反应,最多可生成22.4L气体(标准状况)。写出加热条件下乙与过量NaOH溶液反应的离子方程式 。
(5)乙溶液中所有离子的浓度等式表达式为 。
(1)第二周期,第∨A族  (2)AlO2-+2H2O
(2)AlO2-+2H2O Al(OH)3+OH-
Al(OH)3+OH-
(3)3Cu + 2NO3— + 8H+ = 3Cu2+ + 2NO↑ + 4H2O
(4)


(5)c(NH4+)+c(H+)=2c(CO32-)+c(HCO3-)+c(OH-)
解析试题分析:质子就是H+,X为H;Y最外层电子数是内层电子数的2倍可知Y为C;工业上采用电解法制备的物质一般是K、Ca、Na、Mg、Al,所以W为O、N为Al,则Z为N。(1)N位于元素周期表第二周期VA族,N和H形成18电子分子为N2H4。(2)含铝元素的呈碱性的盐溶液一般是偏铝酸盐。(3)H、C、N、O中三种元素组成强酸为硝酸,铜与稀硝酸生成硝酸铜、一氧化氮和水。(4)H、C、N、O四种元素组成既能与盐酸又能与氢氧化钠溶液反应的物质可能是碳酸铵或碳酸氢铵或氨基酸,由乙与过量浓氢氧化钠溶液反应生成1mol气体可知乙为碳酸氢铵,碳酸氢铵与过量氢氧化钠溶液加热条件下生成碳酸钠、氨气和水。(5)碳酸氢铵溶液中含有NH4+、H+、HCO3-、CO32-、OH-,根据电荷守恒即可得出答案。
考点:元素周期表 元素推断 化学用语 盐类的水解 离子方程式 电荷守恒
点评:工业上电解熔融氯化钠或熔融氢氧化钠制钠、电解熔融氯化镁制镁、电解熔融氧化铝制铝。


 口算题天天练系列答案
口算题天天练系列答案科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:






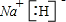
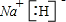
查看答案和解析>>
科目:高中化学 来源: 题型:
 、
、 、
、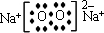
 、
、 、
、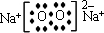
| ||
| ||
查看答案和解析>>
科目:高中化学 来源: 题型:
 已知X、Y、Z、W均为中学化学中常见的单质或化合物,它们之间的转化关系如图所示(部分产物已略去).则W、X不可能是( )
已知X、Y、Z、W均为中学化学中常见的单质或化合物,它们之间的转化关系如图所示(部分产物已略去).则W、X不可能是( )| W | X | |
| A | 盐酸 | Na2CO3溶液 |
| B | NaOH溶液 | AlCl3溶液 |
| C | CO2 | Ca(OH)2溶液 |
| D | O2 | Na |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com