SnCl
4的制备需分两步进行:第一步是金属Sn的制备,第二步由Sn和Cl
2反应生成SnCl
4.
第一步:金属Sn的制备--以锡石SnO
2为原料,用足量的焦炭作还原剂,在高温下可制得粗锡,该反应的化学方程式为
.
已知锡与碳同族,粗锡经电解精炼可得纯锡,精炼时的阴极反应式为
Sn2++2eˉ=Sn
Sn2++2eˉ=Sn
.
第二步:SnCl
4的制备--用干燥、纯净的Cl
2与熔融的Sn反应制SnCl
4,同时放出大量的热.已知SnCl
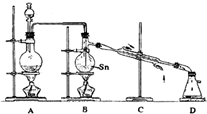
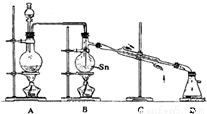
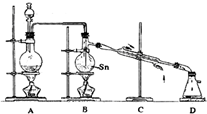
4常温下是无色液体,沸点114℃,遇潮湿空气便发生水解反应,Sn的熔点:231℃,如图1是制取SnCl
4的实验装置.
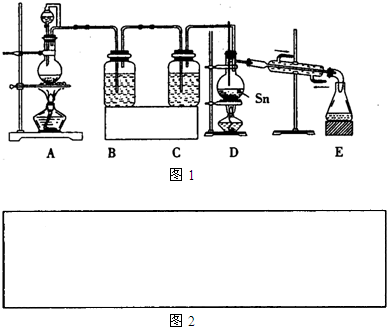
试回答以下问题:
(1)本试验中检查制气装置A气密性的方法是
将A右端导管放人盛有水的烧杯中,微热烧瓶导管口出现气泡,冷却导管中出现一段稳定水柱
将A右端导管放人盛有水的烧杯中,微热烧瓶导管口出现气泡,冷却导管中出现一段稳定水柱
.
装置A中反应的化学方程式为
MnO
2+4HCl(浓)
MnCl
2+Cl
2↑+2H
2O
MnO
2+4HCl(浓)
MnCl
2+Cl
2↑+2H
2O
.
(2)装置B、C中的药品名称分别是
饱和食盐水
饱和食盐水
、
浓硫酸
浓硫酸
.
(3)当反应生成SnCl
4时,应熄灭
D
D
处的酒精灯,理由是
依靠反应放出的热量维持SnCl4的生成
依靠反应放出的热量维持SnCl4的生成
.
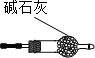
(4)老师说该实验装置E设计仍不完整,请你协助该研究小组设计出所缺装置(须标出试剂的名称,装置图尽可能简单)并在图2的方框中画出.
(5)实验制得的SnCl
4中因溶解了Cl
2而略显黄色.提纯SnCl
4的方法是
蒸馏
蒸馏
.


 ;
;

 名校课堂系列答案
名校课堂系列答案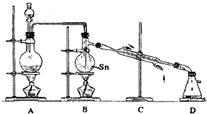 SnCl4的制备需分两步进行,第一步是金属Sn的制备,第二步由Sn和Cl2反应生成SnCl4.
SnCl4的制备需分两步进行,第一步是金属Sn的制备,第二步由Sn和Cl2反应生成SnCl4.
 SnCl4的制备需分两步进行,第一步是金属Sn的制备,第二步由Sn和Cl2反应生成SnCl4.
SnCl4的制备需分两步进行,第一步是金属Sn的制备,第二步由Sn和Cl2反应生成SnCl4.