
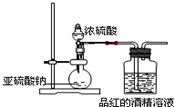
 为探究SO2的漂白是SO2直接作用于有色物质,还是SO2与水反应的产物的作用,设计如图装置进行实验:(图中所用硫酸的质量分数为70%)
为探究SO2的漂白是SO2直接作用于有色物质,还是SO2与水反应的产物的作用,设计如图装置进行实验:(图中所用硫酸的质量分数为70%)分析 发生装置制备的二氧化硫中含有水蒸气,为探究SO2的漂白是SO2直接作用于有色物质,还是SO2与水反应的产物的作用,应将二氧化硫进行干燥;
二氧化硫有毒,直接排放能够引起空气污染;
解答 解:发生装置制备的二氧化硫中含有水蒸气,为探究SO2的漂白是SO2直接作用于有色物质,还是SO2与水反应的产物的作用,应将二氧化硫进行干燥,图中实验装置缺少二氧化硫的干燥装置;二氧化硫有毒,直接排放能够引起空气污染,需要进行尾气处理,图中装置缺少尾气处理装置;
故答案为:①没有干燥装置;②没有吸收尾气的装置;
点评 本题考查了二氧化硫漂白性原理的探究,明确物质的性质是解题关键,注意试验设计的严密性,题目难度不大.


科目:高中化学 来源: 题型:解答题
 ;
;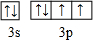 .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 主族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0族 |
| 2 | ① | ② | ③ | |||||
| 3 | ④ | ⑤ | ⑥ | ⑦ | ⑧ | |||
| 4 | ⑨ |
 .
. .
. ,该化合物是由极性(填“极性”或“非极性”)共价键形成的.
,该化合物是由极性(填“极性”或“非极性”)共价键形成的.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
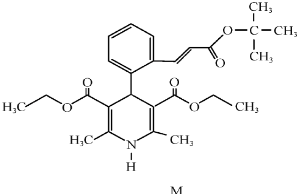
| A. | 属于芳香族化合物 | B. | 遇FeCl3溶液显紫色 | ||
| C. | 不能使酸性高锰酸钾溶液褪色 | D. | 1molM完全水解生成2mol醇 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
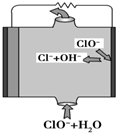 镁燃料电池具有比能量高、使用安全方便、原材料来源丰富、成本低等特点.一般研究的镁燃料电池可分为镁空气燃料电池、镁海水燃料电池、镁过氧化氢燃料电池和镁次氯酸盐燃料电池.其中,镁次氯酸盐燃料电池的工作原理如图所示,下列有关说法不正确的是( )
镁燃料电池具有比能量高、使用安全方便、原材料来源丰富、成本低等特点.一般研究的镁燃料电池可分为镁空气燃料电池、镁海水燃料电池、镁过氧化氢燃料电池和镁次氯酸盐燃料电池.其中,镁次氯酸盐燃料电池的工作原理如图所示,下列有关说法不正确的是( )| A. | 放电过程中OH-移向正极 | |
| B. | 电池的总反应式为Mg+ClO-+H2O═Mg(OH)2+Cl- | |
| C. | 镁燃料电池中镁均为负极,发生氧化反应 | |
| D. | 镁过氧化氢燃料电池,酸性电解质中正极反应式为H2O2+2H++2e-═2H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
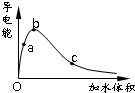 一定温度下,将一定质量的冰醋酸加水稀释过程中,溶液的导电能力变化如图所示:
一定温度下,将一定质量的冰醋酸加水稀释过程中,溶液的导电能力变化如图所示:查看答案和解析>>
科目:高中化学 来源: 题型:解答题
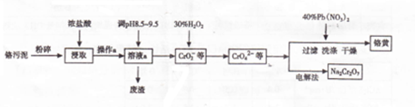
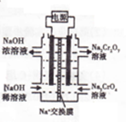
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 在稀氨水中通入过量CO2:NH3•H2O+CO2═NH4++HCO3- | |
| B. | 向(NH4)2SO4溶液中加入适量Ba(OH)2:Ba2++SO42-=BaSO4↓ | |
| C. | 用稀HNO3溶解FeS固体:FeS+2H+═Fe2++H2S↑ | |
| D. | 氢氧化钙溶液与等物质的量的稀硫酸混合:Ca2++OH-+H++SO42-═CaSO4↓+H2O |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com