
”¾ĢāÄæ”æ¼×Ķ¼ĪŖŅ»ÖÖŠĀŠĶĪŪĖ®“¦Ąķ×°ÖĆ£¬øĆ×°ÖĆæÉĄūÓĆŅ»ÖÖĪ¢ÉśĪļ½«ÓŠ»ś·ĻĖ®µÄ»ÆѧÄÜÖ±½Ó×Ŗ»ÆĪŖµēÄÜ£¬ŅŅĶ¼ŹĒŅ»ÖÖÓƶčŠŌµē¼«µē½ā±„ŗĶŹ³ŃĪĖ®µÄĻū¶¾Ņŗ·¢ÉśĘ÷”£¹ŲÓŚ¼×”¢ŅŅµÄĖµ·ØÕżČ·µÄŹĒ
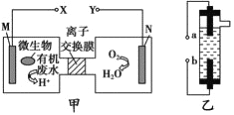
A. ×°ÖĆŅŅÖŠµÄb¼«ŅŖÓė×°ÖĆ¼×µÄX¼«Į¬½Ó
B. ×°ÖĆŅŅÖŠa¼«µÄµē¼«·“Ó¦Ź½ĪŖ:2Cl- -2e-=Cl2”ü
C. µ±N¼«ĻūŗÄ5.6L(±ź×¼×“æöĻĀ)ĘųĢåŹ±£¬ŌņÓŠ2NAøöH+ĶعżĄė×Ó½»»»Ä¤
D. ČōÓŠ»ś·ĻĖ®ÖŠÖ÷ŅŖŗ¬ÓŠĘĻĢŃĢĒ£¬Ōņ×°ÖĆ¼×ÖŠM¼«·¢ÉśµÄµē¼«·“Ó¦ĪŖ: C6H12O6+6H2O-24e-=6CO2”ü+24H+
”¾“š°ø”æD
”¾½āĪö”æÓÉŅŃÖŖ½įŗĻĶ¼Ź¾£¬¼×ĪŖŌµē³Ų£¬XĪŖøŗ¼«”¢YĪŖÕż¼«£¬ŅŅĪŖÓƶčŠŌµē¼«µē½ā±„ŗĶŹ³ŃĪĖ®µÄĻū¶¾Ņŗ·¢ÉśĘ÷£¬ŌņaĪŖŅõ¼«Éś³ÉĒāĘųŗĶNaOH£¬bĪŖŃō¼«Éś³ÉCl2£¬ÓŠĄūÓŚCl2ÓėNaOH·“Ӧɜ³ÉNaClO”£
AĻī£¬bĪŖµē½ā³ŲŃō¼«£¬Ó¦Óėµē³ŲÕż¼«(Y¼«)Į¬½Ó£¬¹ŹA“ķĪó£»BĻī£¬aĪŖŅõ¼«£¬µē¼«·“Ó¦Ź½ĪŖ£ŗ2H2O+2e-=2OH-+H2”ü£¬bĪŖŃō¼«£¬µē¼«·“Ó¦Ź½ĪŖ£ŗ2Cl--2e-=Cl2”ü£¬¹ŹB“ķĪó£»CĻī£¬ČēĶ¼£¬Nµē¼«ĪŖŃõĘųµĆµē×Ó·¢Éś»¹Ō·“Ó¦£¬µē¼«·“Ó¦Ź½ĪŖ£ŗO2+4H++4e-=2H2O£¬Ōņµ±Nµē¼«ĻūŗÄ5.6L(±ź×¼×“æöĻĀ)ĘųĢå(¼“0.25mol)Ź±£¬ĻūŗÄ1molĒāĄė×Ó£¬ŌņÓŠNAøöH+ĶعżĄė×Ó½»»»Ä¤£¬¹ŹC“ķĪó£»DĻī£¬ČōÓŠ»ś·ĻĖ®ÖŠÖ÷ŅŖŗ¬ÓŠĘĻĢŃĢĒ£¬Ōņ×°ÖĆ¼×ÖŠM¼«·¢ÉśC6H12O6Ź§µē×ÓµÄŃõ»Æ·“Ó¦£¬Éś³É¶žŃõ»ÆĢ¼£¬øł¾ŻµēŗÉŹŲŗćŗĶŌ×ÓŹŲŗć£¬Ęäµē¼«Ó¦ĪŖ£ŗC6H12O6+6H2O-24e-=6CO2”ü+24H+£¬¹ŹDÕżČ·”£



| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æ°×Ķ·ĪĢĖŲŃÜÉśĪļHŹĒŅ»ÖÖ¾ßÓŠæ¹¾ś×÷ÓƵĻÆŗĻĪļ£¬ŹµŃéŹŅÓÉ·¼Ļć»ÆŗĻĪļAÖʱøHµÄŅ»ÖÖŗĻ³ÉĀ·ĻßČēĻĀ:
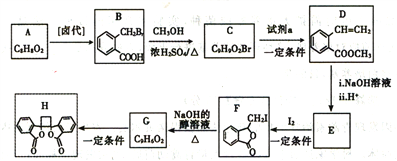
ŅŃÖŖ:i.RCH2Br![]() R-CH=CH-R
R-CH=CH-R
ii.2R-CH=CH-R'![]()
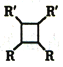 (ŅŌÉĻR”¢R'“ś±ķĒā»ņĢž»łµČ)
(ŅŌÉĻR”¢R'“ś±ķĒā»ņĢž»łµČ)
(1)AµÄ»ÆѧĆū³ĘŹĒ_____________”£CÖŠĖłŗ¬¹ŁÄÜĶŵÄĆū³ĘĪŖ_______________”£
(2)ŹŌ¼ĮaŹĒ____________________£¬GÉś³ÉHµÄ·“Ó¦ĄąŠĶŹĒ_____________________”£
(3)ÓÉFÉś³ÉGµÄ»Æѧ·½³ĢŹ½ŹĒ_______________________________”£
(4)DµÄĶ¬·ÖŅģ¹¹ĢåÖŠ£¬ÄÜĶ¬Ź±Āś×ćĻĀĮŠĢõ¼žµÄ¹²ÓŠ_______ÖÖ(²»ŗ¬Į¢Ģå½į¹¹);
¢Ł±½»·ÉĻÖ»ÓŠĮ½øöČ”“ś»ł
¢ŚÄÜŹ¹äåµÄĖÄĀČ»ÆĢ¼ČÜŅŗĶŹÉ«
¢Ū¼ČÄÜ·¢ÉśŅų¾µ·“Ó¦ÓÖÄÜ·¢ÉśĖ®½ā·“Ó¦ĒŅĖ®½ā²śĪļÖ®Ņ»ÄÜÓėĀČ»ÆĢśČÜŅŗ·¢ÉśĻŌÉ«·“Ó¦£¬ĘäÖŠŗĖ“Ź²ÕńĒāĘ×ĪŖĪå×é·åµÄÓŠ»śĪļµÄ½į¹¹¼ņŹ½ĪŖ_________________________”£
(5)ŅŌŅŅ“¼ĪŖĘšŹ¼ŌĮĻ£¬½įŗĻŅŃÖŖŠÅĻ¢Ń”ÓƱŲŅŖµÄĪŽ»śŹŌ¼ĮŗĻ³É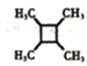 £¬Š“³öŗĻ³ÉĀ·Ļß_________________(ÓĆ¼ņŹ½±ķŹ¾ÓŠ»śĪļ£¬ÓĆ¼żĶ·±ķŹ¾×Ŗ»Æ¹ŲĻµ£¬¼żĶ·ÉĻ×¢Ć÷ŹŌ¼ĮŗĶ·“Ó¦Ģõ¼ž)”£
£¬Š“³öŗĻ³ÉĀ·Ļß_________________(ÓĆ¼ņŹ½±ķŹ¾ÓŠ»śĪļ£¬ÓĆ¼żĶ·±ķŹ¾×Ŗ»Æ¹ŲĻµ£¬¼żĶ·ÉĻ×¢Ć÷ŹŌ¼ĮŗĶ·“Ó¦Ģõ¼ž)”£
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æµĀ¹ś»Æѧ¼Ņ¹ž²®“Ó1902 ÄźæŖŹ¼ŃŠ¾æÓɵŖĘųŗĶĒāĘųÖ±½ÓŗĻ³É°±£¬·“Ó¦ŌĄķĪŖ£ŗN2(g)+3H2(g)![]() 2NH3(g) ”÷H=-92.4kJmol-1
2NH3(g) ”÷H=-92.4kJmol-1
£Ø1£©ŌŚŗćĪĀŗćČŻĢõ¼žĻĀ£¬Ļņ·“Ó¦Ę½ŗāĢåĻµÖŠ³äČėµŖĘų£¬“ļµ½ŠĀĘ½ŗāŹ±£¬c(H2)½«_________(Ģī”°Ōö“ó”±”¢”°¼õŠ””±”¢”°²»±ä”±»ņ”°ĪŽ·ØÅŠ¶Ļ”±£¬ĻĀĶ¬)£¬c(N2)”¤c3(H2)½«___________”£
£Ø2£©¹¤ŅµÉĻæÉÓĆCH4ÓėĖ®ÕōĘųÖĘĒāĘų£ŗCH4(g)+H2O(g)![]() CO(g)+3H2(g)”£ŌŚ200”ꏱ2LµÄĆܱÕČŻĘ÷ÖŠ£¬½«1molCH4ŗĶ1mol H2O(g)»ģŗĻ£¬“ļĘ½ŗāŹ±CH4 µÄ×Ŗ»ÆĀŹĪŖ80%”£Ōņ200”ꏱøĆ·“Ó¦µÄĘ½ŗā³£ŹżK=______________£Ø±£ĮōŅ»Ī»Š”Źż£©”£
CO(g)+3H2(g)”£ŌŚ200”ꏱ2LµÄĆܱÕČŻĘ÷ÖŠ£¬½«1molCH4ŗĶ1mol H2O(g)»ģŗĻ£¬“ļĘ½ŗāŹ±CH4 µÄ×Ŗ»ÆĀŹĪŖ80%”£Ōņ200”ꏱøĆ·“Ó¦µÄĘ½ŗā³£ŹżK=______________£Ø±£ĮōŅ»Ī»Š”Źż£©”£
£Ø3£©ČēĶ¼ĪŖŗĻ³É°±·“Ó¦ŌŚ²»Ķ¬ĪĀ¶ČŗĶŃ¹Ē攢Ź¹ÓĆĻąĶ¬“߻ƼĮĢõ¼žĻĀ£¬³õŹ¼Ź±µŖĘų”¢ĒāĘųµÄĢå»ż±ČĪŖ1:3 Ź±£¬Ę½ŗā»ģŗĻĪļÖŠ°±µÄĢå»ż·ÖŹż”£Čō·Ö±šÓĆvA(NH3)ŗĶvB(NH3)±ķŹ¾“Ó·“Ó¦æŖŹ¼ÖĮ“ļĘ½ŗāדĢ¬A”¢B Ź±µÄ»Æѧ·“Ó¦ĖŁĀŹ£¬ŌņvA(NH3)____ ( Ģī”°>”±”°<”±»ņ”°=”±)vB(NH3)”£

£Ø4£©¹¤ŅµÉś²śÖŠŅŻ³öµÄ°±æÉÓĆĻ”ĮņĖįĪüŹÕ”£ČōĒ”ŗĆÉś³ÉNH4HSO4£¬øĆČÜŅŗÖŠø÷Ąė×ÓµÄĪļÖŹµÄĮæÅضČÓɓ󵽊”µÄĖ³ŠņŹĒ______________________”£
£Ø5£©H2NCOONH4ŹĒ¹¤ŅµŗĻ³ÉÄņĖŲµÄÖŠ¼ä²śĪļ£¬øĆ·“Ó¦µÄÄÜĮæ±ä»ÆČēĶ¼ĖłŹ¾£¬ÓĆCO2ŗĶ°±ŗĻ³ÉÄņĖŲµÄČČ»Æѧ·½³ĢŹ½ĪŖ_________________________________”£
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æ±āĢŅĖįŃÜÉśĪļŹĒÖŲŅŖµÄŅ½Ņ©ÖŠ¼äĢ壬ŅŌA”¢BĪŖŌĮĻŗĻ³É±āĢŅĖįŃÜÉśĪļFĀ·ĻßČēĻĀ£ŗ
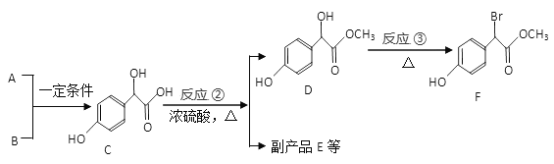
£Ø1£© A µÄ·Ö×ÓŹ½ĪŖC2H2O3£¬1molA ÄÜĻūŗÄŗ¬ÓŠ2.5 molCu(OH)2 ŠĀÖĘŠü×ĒŅŗ£¬Š“³ö·“Ó¦¢ŁµÄ»Æѧ·½³ĢŹ½_______________________________”£
£Ø2£©»ÆŗĻĪļC Ėłŗ¬¹ŁÄÜĶÅĆū³ĘĪŖ______________£¬ŌŚŅ»¶ØĢõ¼žĻĀC Óė×ćĮæNaOH ČÜŅŗ·“Ó¦£¬1molC ×ī¶ąĻūŗÄNaOH µÄĪļÖŹµÄĮæĪŖ_________________mol”£
£Ø3£©·“Ó¦¢ŚµÄ·“Ó¦ĄąŠĶĪŖ___________£» ĒėŠ“³ö·“Ó¦¢ŪµÄ»Æѧ·½³ĢŹ½_____________________________”£
£Ø4£©E ŹĒÓÉ2 øö·Ö×ÓCÉś³ÉµÄŗ¬ÓŠ3 øöĮłŌŖ»·µÄ»ÆŗĻĪļ£¬E µÄ·Ö×ÓŹ½ĪŖ____________________”£
£Ø5£©·ūŗĻĢõ¼žµÄF µÄĖłÓŠĶ¬·ÖŅģ¹¹Ģå(²»æ¼ĀĒĮ¢ĢåŅģ¹¹) ÓŠ__________ÖÖ£¬ĘäÖŠŗĖ“Ź²ÕńĒāĘ×ÓŠĪå×é·åµÄ½į¹¹¼ņŹ½ĪŖ____________________”£
¢ŁŹōÓŚŅ»ŌŖĖįĄą»ÆŗĻĪļ£» ¢Ś±½»·ÉĻÖ»ÓŠ2 øöČ”“ś»ł ¢ŪÓöFeCl3 ČÜŅŗĻŌ×ĻÉ«
£Ø6£©²ĪÕÕÉĻŹöŗĻ³ÉĀ·Ļß”£ŅŌ±ł“×ĖįĪŖŌĮĻ£ØĪŽ»śŹŌ¼ĮČĪŃ”£©Éč¼ĘÖʱøA µÄŗĻ³ÉĀ·Ļß”£¼ŗÖŖRCH2COOH ![]() RCH(Cl)COOH______________________
RCH(Cl)COOH______________________
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æÉś»īÖŠÓŠŠķ¶ąÓė»ÆѧĻą¹ŲµÄŹż¾Ż±ķøń”£
¢ń£®ĻĀĶ¼ŹĒij¶łĶÆĪ¢ĮæŌŖĖŲĢå¼ģ±Øø굄µÄ²æ·ÖŹż¾Ż£ŗijŅ½ĮĘ»ś¹¹ĮŁ“²¼ģŃé½į¹ū±Øø굄
·ÖĪöĻīÄæ | ¼ģ²ā½į¹ū | µ„Ī» | ²Īæ¼·¶Ī§ | |
1 | Šæ£ØZn£© | 115.92 | ¦Ģmol/L | 66~120 |
2 | Ģś£ØFe£© | 6.95 | mmol/L | 7.52~11.82 |
3 | øĘ£ØCa£© | 1.68 | mmol/L | 1.55~2.10 |
”” |
øł¾ŻÉĻ±ķµÄŹż¾Ż£¬»Ų“šĻĀĮŠĪŹĢā£ŗ
(1)øƶłĶÆ__________ŌŖĖŲŗ¬ĮæĘ«µĶ”£
(2)±Øø굄֊”°¦Ģmol/L”±ŹĒ__________£ØĢī”°ÖŹĮæ”±”¢”°Ģå»ż”±»ņ”°ÅØ¶Č”±£©µÄµ„Ī»”£
(3)·žÓĆĪ¬ÉśĖŲCæÉŹ¹Ź³ĪļÖŠµÄFe3+×Ŗ»ÆĪŖFe2+£¬ŌŚÕāøö¹ż³ĢÖŠĢåĻÖĪ¬ÉśĖŲCµÄ__________£ØĢī”°Ńõ»ÆŠŌ”±»ņ”°»¹ŌŠŌ”±£©”£
¢ņ£®Éś»īÖŠĪŖĮĖŃÓ³¤ĻŹ»ØµÄŹŁĆü£¬Ķس£»įŌŚ»ØĘæÖŠ¼ÓČėĻŹ»Ø±£ĻŹ¼Į”£ĻĀ±ķŹĒ0.5LijÖÖĻŹ»Ø±£ĻŹ¼ĮÖŠŗ¬ÓŠµÄ³É·Ö¼°ŗ¬Į棬ŌĶĮŗó»Ų“šĻĀĮŠĪŹĢā£ŗ
³É·Ö | ÖŹĮæ(g) | Ħ¶ūÖŹĮæ(g/mol) |
¢ŁÕįĢĒ£ØC12H22O11£© | 25.00 | 342 |
0.25 | 174 | |
¢ŪøßĆĢĖį¼Ų£ØKMnO4£© | 0.25 | 158 |
¢Ü°¢Ė¾Ę„ĮÖ£ØC9H8O4£© | 0.17 | 180 |
¢ŻĻõĖįŅų£ØAgNO3£© | 0.02 | 170 |
(4)ÉĻŹöĻŹ»Ø±£ĻŹ¼Į³É·ÖÖŠ£¬ŹōÓŚŃĪµÄŹĒ__________£ØĢīŠņŗÅ£©”£
(5)ÓūÅäÖĘ500mLøĆĻŹ»Ø±£ĻŹ¼Į£¬ÓŠČēĻĀ²Ł×÷²½Öč£ŗ
a£®°Ń³ĘĮæŗƵı£ĻŹ¼Į·ÅČėŠ”ÉÕ±ÖŠ£¬¼ÓŹŹĮæÕōĮóĖ®Čܽā£»
b£®°ŃaĖłµĆČÜŅŗŠ”ŠÄ×ŖČė500mLČŻĮæĘæÖŠ£»
c£®¼ĢŠųĻņČŻĮæĘæÖŠ¼ÓÕōĮóĖ®ÖĮŅŗĆę¾ąæĢ¶Č1cm~2cm“¦£¬øÄÓĆ½ŗĶ·µĪ¹ÜŠ”ŠÄµĪ¼ÓÕōĮóĖ®ÖĮČÜŅŗ°¼ŅŗĆę×īµĶ“¦ÓėæĢ¶ČĻßĻąĒŠ£»
d£®ÓĆÉŁĮæÕōĮóĖ®Ļ“µÓÉÕ±ŗĶ²£Į§°ō2~3“Ī£¬Ćæ“ĪĻ“µÓŅŗ¶¼Š”ŠÄ×ŖČėČŻĮæĘ棬²¢ĒįĒįŅ”ŌČ£»
e£®½«ČŻĮæĘæČū½ō£¬·“ø“ÉĻĻĀµßµ¹Ņ”ŌČ”£
¢Ł²Ł×÷²½ÖčµÄÕżČ·Ė³ŠņĪŖ£ØĢīŠņŗÅ£©__________”£
¢ŚŌŚČŻĮæĘæµÄŹ¹ÓĆ·½·ØÖŠ£¬ĻĀĮŠ²Ł×÷²»ÕżČ·µÄŹĒ__________”£
A£®Ź¹ÓĆČŻĮæĘæĒ°¼ģ²éĖüŹĒ·ńĀ©Ė®
B£®ČŻĮæĘæÓĆÕōĮóĖ®Ļ“¾»ŗ󣬊čŅŖøÉŌļ
C£®øĒŗĆĘæČū£¬ÓĆŅ»Ö»ŹÖµÄŹ³Öø¶„×”ĘæČū£¬ĮķŅ»Ö»ŹÖµÄŹÖÖøĶŠ×”Ęæµ×£¬°ŃČŻĮæĘæµ¹×ŖŗĶŅ”¶Æ¼ø“Ī
(6)Š“³öøĆĻŹ»Ø±£ĻŹ¼ĮÖŠK+µÄĪļÖŹµÄĮæÅØ¶ČµÄ¼ĘĖćŹ½c(K+)£½__________ mol”¤L1”£
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æŹÆÓĶĮŃ½āĘųÓĆĶ¾¹ć·ŗ”£ĻĀĆęŹĒŅŌŹÆÓĶĮŃ½āĘųĪŖŌĮĻŗĻ³ÉCRĻš½ŗŗĶŅ½Ņ©ÖŠ¼äĢåKµÄĀ·Ļߣŗ
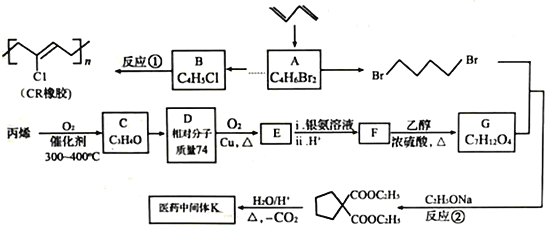
ŅŃÖŖ£ŗ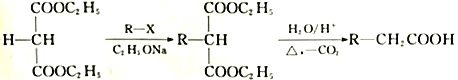
»Ų“šĻĀĮŠĪŹĢā£ŗ
£Ø1£©AµÄĖ³Ź½Ņģ¹¹ĢåµÄ½į¹¹¼ņŹ½ĪŖ________________£¬BµÄ»ÆѧĆū³ĘŹĒ________________”£C·Ö×ÓÖŠĪŽ»·×“½į¹¹£¬Ęä¹ŁÄÜĶÅĆū³ĘĪŖ____________________________”£
£Ø2£©KµÄ½į¹¹¼ņŹ½ĪŖ____________£¬·“Ó¦¢Ł”¢¢ŚµÄ·“Ó¦ĄąŠĶ·Ö±šĪŖ_____________”¢_____________”£
£Ø3£©D”¢EµÄ½į¹¹¼ņŹ½·Ö±šĪŖ_____________”¢_____________”£
£Ø4£©FÓėŅŅ¶ž“¼·¢Éś¾ŪŗĻ·“Ó¦µÄ»Æѧ·½³ĢŹ½ĪŖ_________________________________”£
£Ø5£©Š“³öĶ¬Ź±Āś×ćĻĀĮŠĢõ¼žµÄŅ½Ņ©ÖŠ¼äĢåKµÄĖłÓŠĶ¬·ÖŅģ¹¹ĢåµÄ½į¹¹¼ņŹ½£ŗ_________________________________________________”£
a.ÓėE»„ĪŖĶ¬ĻµĪļ b.ŗĖ“Ź²ÕńĒāĘ×ĻŌŹ¾ĪŖ3×é·å
£Ø6£©ŅŃÖŖĖ«¼üÉĻµÄĒāŌ×ÓŗÜÄŃ·¢ÉśČ”“ś·“Ó¦”£ŅŌAĪŖĘšŹ¼ŌĮĻ£¬Ń”ÓƱŲŅŖµÄĪŽ»śŹŌ¼ĮŗĻ³ÉB£¬Š“³öŗĻ³ÉĀ·Ļߣŗ_______________________________________________”£
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æĢ¼”¢µŖ¼°Ęä»ÆŗĻĪļÓėÉś»īĆÜĒŠĻą¹Ų”£Ēėøł¾ŻŅŖĒó»Ų“šĻĀĮŠĪŹĢā:
£Ø1£©ÓĆCH4“߻ƻ¹ŌµŖŃõ»ÆĪļæÉŅŌĻū³żµŖŃõ»ÆĪļµÄĪŪČ¾”£ŅŃÖŖ:
¢ŁCH4(g)+4NO2(g)= 4NO(g)+CO2(g)+2H2O(g) ”÷H=-574kJ/mol
¢ŚCH4(g)+4NO(g)= 2N2(g)+CO2(g)+2H2O(g) ”÷H=-l160kJ/mol
¢ŪH2O(g)= H2O(l) ”÷H=-44kJ/mol
Š“³öCH4(g)ÓėNO2(g)·“Ӧɜ³ÉN2(g)”¢CO2(g)ŗĶH2O( 1) µÄČČ»Æѧ·½³ĢŹ½_________”£
£Ø2£©ŅŃÖŖ: ·“Ó¦I: 4NH3(g)+5O2(g) ![]() 4NO(g)+6H2O(g) ”÷H < 0
4NO(g)+6H2O(g) ”÷H < 0
·“Ó¦II: 4NH3(g)+3O2(g) ![]() 2N2(g)+6H2O(g) ”÷H < 0
2N2(g)+6H2O(g) ”÷H < 0
¢ŁŌŚŗćĪĀŗćȯװÖĆÖŠ³äČėŅ»¶ØĮæµÄNH3 ŗĶO2,ŌŚ“߻ƼĮµÄ×÷ÓĆĻĀ½ųŠŠ·“Ó¦I£¬ŌņĻĀĮŠÓŠ¹ŲŠšŹöÖŠÕżČ·µÄŹĒ___(Ģī×ÖÄøŠņŗÅ)”£
A.Ōö“óŃ¹Ē棬Kp(ÓĆŃ¹Ēæ±ķŹ¾µÄ»ÆŃ§Ę½ŗā³£Źż) Ōö“ó
B.Čō²āµĆČŻĘ÷ÄŚ3vÕż(NH3)=2vÄę(H2O) Ź±£¬ĖµĆ÷·“Ó¦ŅŃ“ļĘ½ŗā
C.ÉżøßĪĀ¶Č£¬NH3 µÄ×Ŗ»ÆĀŹŌö“ó
D.“ļµ½Ę½ŗāŹ±ĢåĻµµÄŃ¹Ēæ²»ŌŁ±ä»Æ
¢Ś°±“ß»ÆŃõ»ÆŹ±»į·¢ÉśÉĻŹöĮ½øö¾ŗÕł·“Ó¦I”¢II”£ĪŖ·ÖĪöij“߻ƼĮ¶ŌøĆ·“Ó¦µÄŃ”ŌńŠŌ£¬ŌŚ1LĆܱÕČŻĘ÷ÖŠ³äČė1molNH3ŗĶ2molO2£¬µĆÓŠ¹ŲĪļÖŹµÄĮæ¹ŲĻµČēĶ¼£¬øĆ“ß»Æ¼ĮŌŚøßĪĀŹ±Ń”Ōń·“Ó¦_____(Ģī”°I”±»ņ”°II”±)”£
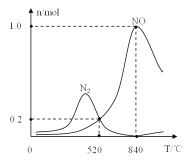
¢Ū520”ꏱ£¬4NH3(g)+3O2 (g)![]() 2N2(g)+6H2O(g)µÄĘ½ŗā³£ŹżK=_______(Ö»ŠčĮŠ³öŹż×Ö¼ĘĖćŹ½)”£ĢįøßNH3×Ŗ»ÆĪŖN2Ę½ŗā×Ŗ»ÆĀŹµÄ“ėŹ©ÓŠ______( Ģī×ÖÄøŠņŗÅ)
2N2(g)+6H2O(g)µÄĘ½ŗā³£ŹżK=_______(Ö»ŠčĮŠ³öŹż×Ö¼ĘĖćŹ½)”£ĢįøßNH3×Ŗ»ÆĪŖN2Ę½ŗā×Ŗ»ÆĀŹµÄ“ėŹ©ÓŠ______( Ģī×ÖÄøŠņŗÅ)
A.½µµĶ·“Ó¦ĪĀ¶Č B.½«·“Ӧɜ³ÉµÄH2O(g)¼°Ź±ŅĘ³ö
C.Ōö“óNH3ŗĶO2µÄ³õŹ¼Ķ¶ĮĻ±Č D.Ķ¶ĮĻ±Č²»±ä£¬Ōö¼Ó·“Ó¦ĪļµÄÅضČ
£Ø3£©¼ŗÖŖ25”ꏱHCN ŗĶH2CO3µÄµēĄė³£Źż(Ka.)ČēĻĀ±ķ:
ĪļÖŹ | µēĄė³£Źż(Ka) |
HCN | Ka=5”Į10-10 |
H2CO3 | Ka1=4.5”Į10-7£»Ka2=4.7”Į 10-11 |
25”ꏱ£¬²āµĆHCN ŗĶNaCN µÄ»ģŗĻČÜŅŗpH=11,Ōņc(HCN)/c(CN-)=____”£ĻņNaCN ČÜŅŗÖŠĶØČėÉŁĮæCO2£¬Ōņ·¢Éś·“Ó¦µÄĄė×Ó·½³ĢŹ½ĪŖ:__________”£
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æ(1)³żČ„Fe(OH)3½ŗĢåÖŠ»ģÓŠµÄFeCl3µÄ·½·ØŹĒ_________________”£
(2)ŌŚŅ»¶ØĢõ¼žĻĀ£¬Ä³¹ĢĢ¬»ÆŗĻĪļXŹÜČČ·Ö½āµÄ·“Ó¦ĪŖ£ŗ2X ![]() A”ü£«B”ü£«2C”ü£¬²āµĆ·“Ó¦ŗóÉś³ÉµÄ»ģŗĻĘųĢåµÄĆܶȏĒĶ¬ĪĀĶ¬Ń¹ĻĀH2ĆܶȵÄ12±¶£¬Ōņ»ÆŗĻĪļXµÄĦ¶ūÖŹĮæĪŖ_______”£
A”ü£«B”ü£«2C”ü£¬²āµĆ·“Ó¦ŗóÉś³ÉµÄ»ģŗĻĘųĢåµÄĆܶȏĒĶ¬ĪĀĶ¬Ń¹ĻĀH2ĆܶȵÄ12±¶£¬Ōņ»ÆŗĻĪļXµÄĦ¶ūÖŹĮæĪŖ_______”£
(3)½«±ź×¼×“æöĻĀµÄa L HClĘųĢåČÜÓŚ1 LĖ®ÖŠ£¬µĆµ½µÄŃĪĖįĆܶČĪŖb g/cm3£¬ŌņøĆŃĪĖįµÄĪļÖŹµÄĮæÅضČĪŖ________________”£
(4)ĻÖӊijĪĀ¶ČĻĀ±„ŗĶNaClČÜŅŗV mL£¬ĆܶČĪŖ¦Ńgcm-3£¬ĪļÖŹµÄĮæÅضČĪŖC molL-1ŌņøĆĪĀ¶ČĻĀNaClµÄČܽā¶ČĪŖ_________________£ØÓĆV”¢¦Ń”¢C±ķŹ¾£©”£
(5)ÓŠA”¢B”¢C”¢D ĖÄÖÖæÉČÜŠŌŃĪ£¬ĖüĆĒµÄŃōĄė×ÓŹĒBa2+”¢Ag+”¢Na+”¢Cu2+ ÖŠµÄijŅ»ÖÖ£¬ŅõĄė×ÓŹĒNO3-”¢SO42-”¢Cl-”¢CO32- µÄijŅ»ÖÖ”£
¢ŁČō°ŃĖÄÖÖŃĪ·Ö±šČܽāÓŚŹ¢ÓŠÕōĮóĖ®µÄĖÄÖ»ŹŌ¹ÜÖŠ£¬CŃĪµÄČÜŅŗ³ŹĄ¶É«”£
¢ŚČōĻņ¢ŁµÄĖÄÖ»ŹŌ¹ÜÖŠ·Ö±š¼ÓŃĪĖį£¬BČÜŅŗÓŠ³Įµķ²śÉś£¬DČÜŅŗÓŠĪŽÉ«ĪŽĪ¶ĘųĢåŅŻ³ö”£
øł¾Ż¢Ł¢ŚŹµŃéŹĀŹµæÉĶʶĻĖüĆĒµÄ»ÆѧŹ½ĪŖ£ŗ
AӢ____________ CӢ______________ DӢ______________
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æĒėøł¾ŻĪļÖŹµÄĮæĻą¹Ų¼ĘĖćĢīæÕ
(1)19.6 g ĮņĖįŹĒ_____mol H2SO4 £¬1.7 gNH3 ŌŚĶ¬ĪĀĶ¬Ń¹ĻĀÓė_____g H2S ĘųĢåŗ¬ÓŠµÄĒāŌ×ÓŹżĻąĶ¬”£
(2)ŌŚ±ź×¼×“æöĻĀ£¬1.6 g ijĘųĢ¬Ńõ»ÆĪļ RO2 Ģå»żĪŖ 0.56L£¬øĆĘųĢåµÄĪļÖŹµÄĮæŹĒ_____£¬R µÄĻą ¶ŌŌ×ÓĮæĪŖ_____”£
(3)ŅŃÖŖ Wg ĘųĢå A ŗ¬ÓŠ a øö·Ö×Ó£¬ÄĒĆ“ŌŚ±ź×¼×“æöĻĀ£¬bg ĘųĢå A ĖłÕ¼µÄĢå»żŹĒ _____L £ØĘäÖŠ°¢ ·ü¼ÓµĀĀŽ³£ŹżÓĆ NA ±ķŹ¾£©
(4)±ź×¼×“æöĻĀ£¬ĆܶČĪŖ 0.75g/L µÄ NH3 Óė CH4 ×é³ÉµÄ»ģŗĻĘųĢåÖŠ£¬NH3 µÄĢå»ż·ÖŹż_______________£¬ »ģŗĻĘųĢåµÄĘ½¾łÄ¦¶ūÖŹĮæĪŖ_____£¬ øĆĘųĢå¶ŌĒāĘųµÄĻą¶ŌĆܶČĪŖ__________________”£
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com