
科目:高中化学 来源: 题型:阅读理解



查看答案和解析>>
科目:高中化学 来源: 题型:
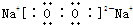
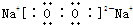
查看答案和解析>>
科目:高中化学 来源: 题型:
| J | ||||
| M | R |
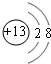

| 选项 | a | b | c | d |
| x | 温度 | 加入H2的物质的量 | 加入H2的物质的量 | 加入甲的物质的量 |
| y | 甲的物质的量 | 平衡常数K | 甲的转化率 | 生成物物质的量总和 |
| ||
| ||
查看答案和解析>>
科目:高中化学 来源: 题型:
A、
| ||||
B、CO2的分子模型: | ||||
| C、在CS2、PCl3中各原子最外层均能达到8电子的稳定结构 | ||||
| D、熵增加且放热的反应一定是自发反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:
下列说法中正确的是
A.外围电子构型为4f75d16s2元素在周期表中的位置是在第四周期第VIII族
B.在氢原子电子云图中通常用小黑点来表示电子的多少,黑点密度大则电子数目多
C.CsCl晶体中与每个Cs+ 距离相等且最近的Cs+共有6个;
D.金刚石立体网状结构中,最小的碳环上有4个碳原子且每个碳原子被6个碳环所共用
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com