
分析 (1)加入固体NaOH,消耗氢离子,促进电离;
(2)加入固体NaClO,次氯酸根离子浓度增大,抑制电离;
(3)因为电离为吸热过程,所以升高温度,电离平衡向正反应方向移动;
(4)NaClO水解属于吸热反应.
解答 解:(1)加入固体NaOH,消耗氢离子,电离平衡向正反应方向移动,则c(H+)减小,故答案为:正;减小;
(2)加入固体NaClO,次氯酸根离子浓度增大,所以电离平衡向逆反应方向移动,c(H+)减小,故答案为:逆;减小;
(3)因为电离为吸热过程,所以升高温度,电离平衡向正反应方向移动,c(H+)增大,故答案为:正;增大;
(4)NaClO水解属于吸热反应,所以NaClO水解的化学方程式为NaClO+H2O?HClO+NaOH,故答案为:吸热;NaClO+H2O?HClO+NaOH;
点评 本题考查电离平衡的移动,明确影响平衡移动的因素即可解答,注意利用加入固体NaOH促进电离及同离子效应来分析解答.


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:选择题
| A. | CO32-Cl- Na+ H+ | B. | K+ Na+ SO42- Ba2+ | ||
| C. | Cl- Na+ Ag+ NO3- | D. | CO32- SO42- Cl- OH- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 臭氧能对水体消毒,是因为其能杀死水中的病菌 | |
| B. | 执行“限塑令”主要是为了节约资源 | |
| C. | 含磷洗涤剂因为其易被细菌分解,所以不会导致水体污染 | |
| D. | 新装修的住房中放置任何花卉都能降低居室中甲醛的含量 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 0.04 | B. | 0.04mol/(L.s) | C. | 0.08mol(L.s) | D. | 0.04mol/L |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
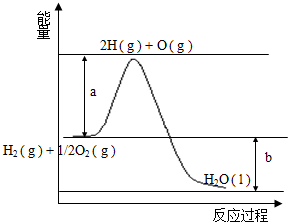 已知H2的燃烧热为285.8kJ•mol-1,反应过程中能量变化如图:请回答下列问题:
已知H2的燃烧热为285.8kJ•mol-1,反应过程中能量变化如图:请回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

| 实验步骤 | 预期现象和结论 |
| 步骤1:取适量产品加适量蒸馏水配成稀溶液,滴加足量BaCl2溶液. | |
| 步骤2: |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com