


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
 某同学设计了如下方案,来测定过氧化钠的样品的纯度(杂质不参加反应,条件为标准状况).
某同学设计了如下方案,来测定过氧化钠的样品的纯度(杂质不参加反应,条件为标准状况).查看答案和解析>>
科目:高中化学 来源: 题型:
| A、单质硅常用做半导体材料和光导纤维,SiO2是人类将光能转化为电能的常用材料 |
| B、纯碱、烧碱、Al(OH)3等常用于治疗胃酸过多 |
| C、H2O2、Na2O2、氯水、漂白粉、84消毒液均可作漂白剂和消毒剂,且它们的漂白原理相同 |
| D、镁铝合金常用于制作窗框是因为它具有坚硬、密度小、溶点高、耐腐蚀等优良性能 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、使酚酞试液变红的溶液:Na+、Cl-、SO42-、Fe3+ |
| B、使紫色石蕊试液变红的溶液:Fe2+、Mg2+、NO3-、Cl- |
| C、碳酸氢钠溶液:K+、SO42-、Cl-、H+ |
| D、c(H+)=10-12 mol?L-1的溶液:K+、Ba2+、Cl-、Br- |
查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:

 )
)查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:
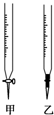 温州某学生用0.1000mol/L NaOH溶液滴定未知浓度的盐酸溶液,其操作可分解为如下几步:
温州某学生用0.1000mol/L NaOH溶液滴定未知浓度的盐酸溶液,其操作可分解为如下几步:| 滴定次数 | 待测液体积/mL | 标准溶液的体积/mL | ||
| 滴定前刻度 | 滴定后刻度 | |||
| 1 | 20 | 1.02 | 21.03 | |
| 2 | 20 | 2.00 | 25.00 | |
| 3 | 20 | 0.60 | 20.59 | |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com