
有关元素A、B、C、D、E的信息如下:
| 元素 | 有关信息 |
| A | 元素主要化合价为-2,A的一种氢化物可用于实验室制取A的单质 |
| B | 所在主族序数与所在周期序数之差为4 |
| C | 原子中含10个P电子 |
| D | 最高价氧化物对应的水化物,能电离出电子数相等的阴、阳离子 |
| E | 生活中常见金属,它有两种氯化物,相对原子质量相差35.5 |
请回答下列问题:
 (1)元素A~E中两种元素组成的化合物使品红溶液褪色的物质的化学式为______。
(1)元素A~E中两种元素组成的化合物使品红溶液褪色的物质的化学式为______。
(2)E元素与B元素可形成EB2和EB3两种化合物,下列说法正确的是(填序号)________。
①保存EB2溶液时,需向溶液中加入少量E单质
②EB2只能通过置换反应生成,EB3只能通过化合反应生成
③铜片、碳棒和EB3溶液组成原电池,电子由铜片沿导线流向碳棒
④向淀粉碘化钾溶液和苯酚溶液中分别滴加几滴EY3的浓溶液,原无色溶液都变为紫色
(3)用化学符号表示D2C的水溶液中各粒子的浓度关系,如c(C2-)=______________。
(4)将一定量的B单质通入一定浓度的苛性钾溶液中,两者恰好完全反应(已知反应过程放热),生成物中含有三种含B元素的离子,其中两种离子的物质的量(n)与反应时间(t)的变化示意图如下图所示。该苛性钾溶液中KOH的质量是___________,该反应中转移电子的物质的量是_________。
(5)工业上冶炼E单质的化学方程式为__________________________________。
(1)SO2、Na2O2(各2分)
(2)①③(3分)
(3)c(S2-)= 1/2[c(Na+)+c(H+)- c(HS-)-c(OH-)]或c(S2-)= 1/2c(Na+)- c(HS-)-c(H2S)(其它合理答案也可)(2分)
(4)16.8g (2分),0.21mol(2分)
(5)Fe2O3+3CO![]() 3CO2+2Fe(3分)
3CO2+2Fe(3分)
根据题给信息A为氧元素,实验室可以用双氧水来制备氧气;所在主族序数与所在周期序数之差为4,B元素为氧或者氯,因为A为氧,所以B为氯元素;C元素原子中含10个P电子,P电子一定为2p63p4,C元素为硫;最高价氧化物对应水化物,能电离出电子数相等的阴、阳离子,由于Mg(OH)2、Al(OH)3难溶,所以该物质为NaOH,D为钠元素;E有两种氯化物,相对原子质量相差35.5,E有变价,为Fe元素。
(1))漂白性物质包括化合漂白和氧化性漂白等,这几种元素中的两种元素形成的具有漂白性的物质有SO2、Na2O2。
(2)FeCl2可以通过化合反应制得,如:2FeCl3+Fe=3FeCl2,FeCl3可以通过分解反应制得如2Fe(OH)3=Fe2O3+3H2O;淀粉碘化钾溶液中滴加几滴FeCl3的浓溶液,溶液呈蓝色,苯酚溶液中滴加几滴FeCl3的浓溶液,溶液显紫色,正确的说法为①③。
 (3)在Na2S溶液中,根据电荷守恒有:2c(S2-)+ c(HS-)+c(OH-)= c(Na+)+c(H+),根据物料守恒有:c(Na+) = 2 [c(S2-)+c(HS-)+c(H2S)],变形即可。
(3)在Na2S溶液中,根据电荷守恒有:2c(S2-)+ c(HS-)+c(OH-)= c(Na+)+c(H+),根据物料守恒有:c(Na+) = 2 [c(S2-)+c(HS-)+c(H2S)],变形即可。
(4)根据得失电子守恒,Cl2与KOH反应生成KClO、KClO3外,还有KCl生成,依据ClO—和ClO3—的物质的量配平方程式,有5Cl2+10KOH=7KCl+2KClO+KClO3+5H2O,转移电子0.03×7=0.21mol,反应消耗KOH的质量为0.03×10×56=16.8g。
(5)工业炼铁是用CO还原铁矿石制得。
本题是以物质结构和元素周期律为载体考查元素及其化合物及基本理论知识。


科目:高中化学 来源: 题型:阅读理解
| 元 素 | 有关信息 |
| A | 最高价氧化物对应的水化物(甲)能与其气态氢化物(乙)反应生成盐 |
| B | 地壳中含量最高的元素,A与B可形成一种质量比为 7:12的化合物(丙) |
| C | 单质曾用于焊接钢轨 |
| D | 单质是生活中常见金属,其制品在自然环境中被腐蚀呈现红棕色 |
| ||
| ||
 容器中,反应过程中各物质的物质的量浓度c随时间t的变化关系如图所示.
容器中,反应过程中各物质的物质的量浓度c随时间t的变化关系如图所示.查看答案和解析>>
科目:高中化学 来源: 题型:
| 元 素 | 有关信息 |
| A | 最高价氧化物对应的水化物(甲)能与其气态氢化物(乙)反应生成盐 |
| B | 最外层电子数是次外层电子数的2倍 |
| C | M层上有3个电子 |
| D | 短周期原子半径最大的主族元素 |
| E | 最高正价与最低负价代数和为6 |

 A2O4(g);△H<0.在恒温恒容条件下,将一定量AO2和A2O4的混合气体通入容积为2L的密闭容器中,反应过程中各物质的物质的量浓度c随时间t的变化关系如下图所示.
A2O4(g);△H<0.在恒温恒容条件下,将一定量AO2和A2O4的混合气体通入容积为2L的密闭容器中,反应过程中各物质的物质的量浓度c随时间t的变化关系如下图所示.查看答案和解析>>
科目:高中化学 来源: 题型:阅读理解
(15分)有关元素A.B.C.D的信息如下:
| 元 素 | 有关信息 |
| A | 最高价氧化物对应的水化物(甲)能与其气态氢化物(乙)反应生成盐 |
| B | 地壳中含量最高的元素,A与B可形成一种质量比为 7︰12的化合物(丙) |
| C | 单质曾用于焊接钢轨 |
| D | 单质是生活中常见金属,其制品在自然环境中被腐蚀呈现红棕色 |
请回答下列问题:
(1)乙分子的空间构型________,用电子式表示乙的形成过程____________________。
(2)有关C与D元素,下列说法正确的是____________________ (填序号)。
①C或D的高价盐均可用做净水剂
②用C或D单质做成的槽车,都可用来运输甲的稀溶液
③C、D的单质与稀硫酸组成的原电池,C电极发生氧化反应
④C的合金可用来做车船材料和门窗等
(3)B的一种氢化物在碱性溶液中可与丙反应,生成物中A元素只显其最高价态,该反应的离子方程式是________________________________________。
(4)现取1 mol/L 100 mL的C的氯化物溶液,向其中加入1 mol/L氢氧化钠溶液产生了3.9 g的沉淀,则加入的氢氧化钠溶液体积可能是____________________mL。
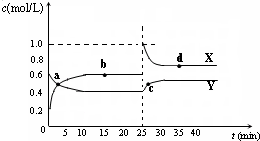
(5)已知:2AB2(g) A2B4(g);△H<0。在恒温恒容条件下,将一定量AB2和A2B4的混合气体通入容积为2L的密闭容器中,反应过程中各物质的物质的量浓度c随时间t的变化关系如下图所示。

① a、b、c、d四个点中,化学反应处于平衡状态的是_______点。
② 25 min时,增加了_______(填物质的化学式)________mol。
③a、b、c、d四个点所表示的反应体系中,气体颜色由深到浅的顺序是_______(填字母)。
查看答案和解析>>
科目:高中化学 来源:2010年河北省唐山一中高三上学期期中考试化学卷 题型:填空题
(15分)有关元素A.B.C.D的信息如下:
| 元素 | 有关信息 |
| A | 最高价氧化物对应的水化物(甲)能与其气态氢化物(乙)反应生成盐 |
| B | 地壳中含量最高的元素,A与B可形成一种质量比为 7︰12的化合物(丙) |
| C | 单质曾用于焊接钢轨 |
| D | 单质是生活中常见金属,其制品在自然环境中被腐蚀呈现红棕色 |
 可能是____________________mL。
可能是____________________mL。 A2B4(g);△H<0。在恒温恒容条件下,将一定量AB2和A2B4的混合气体通入容积为2L的密闭容器中,反应过程中各物质的物质的量浓度c随时间t的变化关系如下图所示。
A2B4(g);△H<0。在恒温恒容条件下,将一定量AB2和A2B4的混合气体通入容积为2L的密闭容器中,反应过程中各物质的物质的量浓度c随时间t的变化关系如下图所示。
 ① a、b、c、d四个点中,化学反应处于平衡状态的是_______点。
① a、b、c、d四个点中,化学反应处于平衡状态的是_______点。查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com