
 2 NH3��g����ƽ��ʱ������干7 mol����a��b��c�ֱ����N2��H2��NH3��ʼ��������ʵ�����ά���¶Ȳ��䣬ʹ�ﵽƽ��ʱ���ɷֵİٷֺ������䣮��
2 NH3��g����ƽ��ʱ������干7 mol����a��b��c�ֱ����N2��H2��NH3��ʼ��������ʵ�����ά���¶Ȳ��䣬ʹ�ﵽƽ��ʱ���ɷֵİٷֺ������䣮�� ��ĩ���ƾ�ϵ�д�
��ĩ���ƾ�ϵ�д� ���ɿ��ñ���ϵ�д�
���ɿ��ñ���ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
 ,2min��Ӧ�ﵽƽ�⣬ AΪ0.4mol�����ı䷴Ӧ����ʱ������ͼ�ı仯��P0��ʾ1������ѹ���������������в���ȷ����
,2min��Ӧ�ﵽƽ�⣬ AΪ0.4mol�����ı䷴Ӧ����ʱ������ͼ�ı仯��P0��ʾ1������ѹ���������������в���ȷ����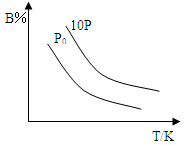
| A��0~2minʱ����B���ʵ�ƽ����Ӧ����Ϊ0.03mol/(L��min) |
| B���÷�Ӧ������Ӧ�Ƿ��ȷ�Ӧ����CΪ���������� |
| C���ﵽƽ������¶Ⱥ�����������䣬�ٳ���1 molA�� ƽ��������Ӧ�����ƶ� |
D�����¶Ⱥ�����������䣬��ʼʱ����B��C��0.5mol ,��ﵽƽ��ʱ,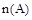 С��0.4mol С��0.4mol |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
A��C(s)+CO2(g) 2CO(g) 2CO(g) | B��3H2(g)+N2(g) 2NH3(g) 2NH3(g) |
C��H2(g)+I2(g) 2HI(g) 2HI(g) | D��C(s)+H2O(g) CO(g) + H2(g) CO(g) + H2(g) |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ������
 FeO��s����CO��g������֪938Kʱƽ�ⳣ��K��1��47��1173Kʱƽ�ⳣ��K��2��15��
FeO��s����CO��g������֪938Kʱƽ�ⳣ��K��1��47��1173Kʱƽ�ⳣ��K��2��15��
 �ٴ�ͼ�п��Կ�������Ӧt2ʱ�ﵽƽ�⣬��
�ٴ�ͼ�п��Կ�������Ӧt2ʱ�ﵽƽ�⣬���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A��0.34 | B��0.64 | C��0.44 | D��0.54 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ������
 FeO(s)��CO(g)����ƽ�ⳣ��ΪK1����ѧ��Ӧ�ڣ�Fe(s)��H2O(g)
FeO(s)��CO(g)����ƽ�ⳣ��ΪK1����ѧ��Ӧ�ڣ�Fe(s)��H2O(g)  FeO(s)��H2(g)����ƽ�ⳣ��ΪK2�����¶�973 K��1 173 K����£�K1��K2��ֵ�ֱ����£�
FeO(s)��H2(g)����ƽ�ⳣ��ΪK2�����¶�973 K��1 173 K����£�K1��K2��ֵ�ֱ����£�| �¶� | K1 | K2 |
| 973 K | 1.47 | 2.38 |
| 1173 K | 2.15 | 1.67 |
 �ƶϣ���Ӧ���� (����ȡ����ȡ�)��Ӧ��
�ƶϣ���Ӧ���� (����ȡ����ȡ�)��Ӧ�� CO(g)��H2O(g)������д���÷�Ӧ��ƽ�ⳣ��K3����ѧ����ʽ��K3�� �����ݷ�Ӧ����ڿ��Ƶ���K1��K2��K3֮��Ĺ�ϵʽ ���ݴ˹�ϵʽ���ϱ����ݣ�Ҳ���ƶϳ���Ӧ��
CO(g)��H2O(g)������д���÷�Ӧ��ƽ�ⳣ��K3����ѧ����ʽ��K3�� �����ݷ�Ӧ����ڿ��Ƶ���K1��K2��K3֮��Ĺ�ϵʽ ���ݴ˹�ϵʽ���ϱ����ݣ�Ҳ���ƶϳ���Ӧ�� �� (����ȡ����ȡ�)��Ӧ��
�� (����ȡ����ȡ�)��Ӧ��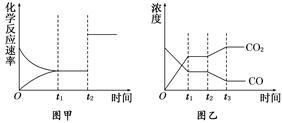
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
 NO��g��+CO2��g�����ﵽ��ѧƽ�⣬������50����CO ת��ΪCO2���������������������£�����1molCO ��2 molNO2 �������������У���Ӧ�ﵽ��ѧƽ��ʱ����������е�CO2�����������
NO��g��+CO2��g�����ﵽ��ѧƽ�⣬������50����CO ת��ΪCO2���������������������£�����1molCO ��2 molNO2 �������������У���Ӧ�ﵽ��ѧƽ��ʱ����������е�CO2�����������| A��1/9 | B��1/6 | C��2/9 | D��1/3 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ������
 CO(g)+ H2O(g)����ƽ�ⳣ��K���¶�T�Ĺ�ϵ�����ʾ��
CO(g)+ H2O(g)����ƽ�ⳣ��K���¶�T�Ĺ�ϵ�����ʾ��| T/�� | 70 0 0 | 800 | 830 | 1000 | 1200 |
| K | 0.6 | 0.9 | 1.0 | 1.7 | 2.6 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ������
 2SO2+O2?2NO+O2
2SO2+O2?2NO+O2 2NO2?
2NO2?�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com